Mpito wa adiabatic kati ya majimbo mawili katika gesi sio moja ya isoprocesses, hata hivyo, ina jukumu muhimu sio tu katika michakato mbalimbali ya teknolojia, lakini pia katika asili. Katika makala haya, tutazingatia mchakato huu ni nini, na pia kutoa milinganyo ya adiabatic kwa gesi bora.
Gesi bora kwa kifupi
Gesi bora ni ile ambayo hakuna mwingiliano kati ya chembe zake, na saizi zake ni sawa na sifuri. Kwa asili, bila shaka, hakuna asilimia mia moja ya gesi bora, kwa kuwa zote zinajumuisha molekuli na atomi za ukubwa, ambazo daima huingiliana angalau kwa msaada wa vikosi vya van der Waals. Hata hivyo, muundo uliofafanuliwa mara nyingi hutekelezwa kwa usahihi wa kutosha wa kutatua matatizo ya vitendo kwa gesi nyingi halisi.
Mlinganyo mkuu wa gesi bora ni sheria ya Clapeyron-Mendeleev. Imeandikwa kwa namna ifuatayo:
PV=nRT.
Mlinganyo huu unathibitisha uwiano wa moja kwa moja kati ya bidhaashinikizo P kwenye kiasi cha V na kiasi cha dutu n kwenye halijoto kamili T. Thamani ya R ni gesi isiyobadilika, ambayo ina jukumu la kipengele cha uwiano.
Mchakato wa adiabatic ni nini?
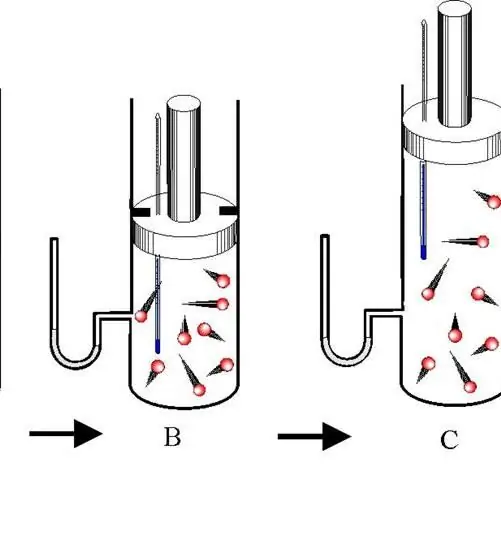
Mchakato wa adiabatic ni mpito kati ya hali ya mfumo wa gesi ambapo hakuna kubadilishana nishati na mazingira. Katika hali hii, sifa zote tatu za thermodynamic za mfumo (P, V, T) hubadilika, na kiasi cha dutu n hubakia bila kubadilika.
Tofautisha kati ya upanuzi wa adiabatic na mkazo. Michakato yote miwili hutokea tu kutokana na nishati ya ndani ya mfumo. Kwa hiyo, kutokana na upanuzi, shinikizo na hasa joto la mfumo hupungua kwa kasi. Kinyume chake, mgandamizo wa adiabatic husababisha kuruka chanya kwa halijoto na shinikizo.
Ili kuzuia ubadilishanaji wa joto kati ya mazingira na mfumo, mfumo wa pili lazima uwe na kuta zenye maboksi ya joto. Aidha, kufupisha muda wa mchakato hupunguza kwa kiasi kikubwa mtiririko wa joto kutoka kwa mfumo.
Milinganyo ya Poisson kwa mchakato wa adiabatic

Sheria ya kwanza ya thermodynamics imeandikwa kama ifuatavyo:
Q=ΔU + A.
Kwa maneno mengine, joto Q linalowasilishwa kwa mfumo hutumika kufanya kazi A na mfumo na kuongeza nishati yake ya ndani ΔU. Ili kuandika equation ya adiabatic, mtu anapaswa kuweka Q=0, ambayo inalingana na ufafanuzi wa mchakato unaojifunza. Tunapata:
ΔU=-A.
Na isochoricmchakato katika gesi bora, joto zote huenda kuongeza nishati ya ndani. Ukweli huu unaturuhusu kuandika usawa:
ΔU=CVΔT.
Ambapo CV ni uwezo wa joto wa isochoriki. Kazi A, kwa upande wake, inakokotolewa kama ifuatavyo:
A=PdV.
Ambapo dV ni badiliko ndogo la sauti.
Mbali na mlinganyo wa Clapeyron-Mendeleev, mlinganyo ufuatao unashikilia gesi bora:
CP- CV=R.
Ambapo CP ni uwezo wa joto wa isobariki, ambao daima ni mkubwa zaidi kuliko isochoriki, kwa kuwa huzingatia hasara za gesi kutokana na upanuzi.
Kuchanganua milinganyo iliyoandikwa hapo juu na kuunganisha juu ya halijoto na sauti, tunafikia mlinganyo wa adiabatic ufuatao:
TVγ-1=const.
Hapa γ ni faharasa ya adiabatic. Ni sawa na uwiano wa uwezo wa joto wa isobaric kwa isochoric. Usawa huu unaitwa equation ya Poisson kwa mchakato wa adiabatic. Kwa kutumia sheria ya Clapeyron-Mendeleev, unaweza kuandika misemo miwili zaidi inayofanana, tu kupitia vigezo P-T na P-V:
TPγ/(γ-1)=const;
PVγ=const.
grafu ya Adiabatic inaweza kutolewa katika shoka tofauti. Hapa chini inaonyeshwa katika shoka za P-V.
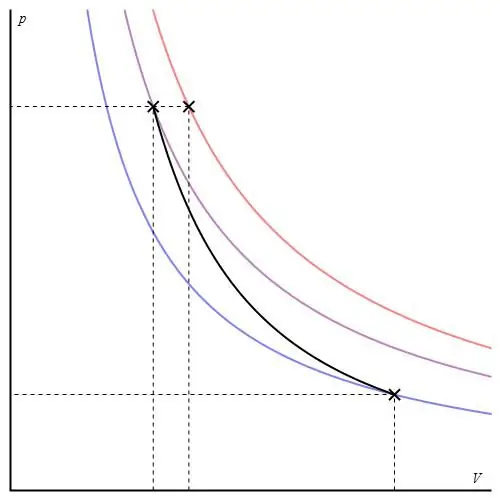
Mistari yenye rangi kwenye grafu inalingana na isothermu, mkunjo mweusi ni adiabat. Kama inavyoonekana, adiabat hutenda kwa kasi zaidi kuliko isotherms yoyote. Ukweli huu ni rahisi kuelezea: kwa isotherm, shinikizo hubadilika nyumasawia na kiasi, lakini kwa isobath, shinikizo hubadilika kwa kasi, kwani kielelezo ni γ>1 kwa mfumo wowote wa gesi.
Tatizo la mfano
Kwa asili, katika maeneo ya milimani, wakati wingi wa hewa unaposonga juu ya mteremko, shinikizo lake hupungua, huongezeka kwa sauti na kupoa. Mchakato huu wa adiabatic hupunguza kiwango cha umande na kutoa mvua ya kioevu na dhabiti.

Inapendekezwa kutatua tatizo lifuatalo: katika mchakato wa kuinua wingi wa hewa kwenye mteremko wa mlima, shinikizo lilishuka kwa 30% ikilinganishwa na shinikizo kwenye mguu. Joto lake lilikuwa sawa na nini ikiwa miguuni lilikuwa 25 oC?
Ili kutatua tatizo, tumia mlingano wa adiabatic ufuatao:
TPγ/(γ-1)=const.
Ni bora kuiandika katika fomu hii:
T2/T1=(P2/P 1)(γ-1)/γ.
Ikiwa P1 itachukuliwa kama angahewa 1, basi P2 itakuwa sawa na angahewa 0.7. Kwa hewa, index ya adiabatic ni 1.4, kwani inaweza kuchukuliwa kuwa gesi bora ya diatomic. Thamani ya halijoto ya T1 ni 298.15 K. Tukibadilisha nambari hizi zote kwenye usemi ulio hapo juu, tunapata T2=269.26 K, ambayo inalingana na - 3, 9 oC.






