Nadharia ya Molekuli-kinetiki inaruhusu, kwa kuchanganua tabia ya hadubini ya mfumo na kutumia mbinu za ufundi wa takwimu, kupata sifa muhimu za makroskopu za mfumo wa thermodynamic. Moja ya sifa za microscopic, ambayo inahusiana na joto la mfumo, ni wastani wa kasi ya mraba ya molekuli za gesi. Tunatoa fomula yake na kuizingatia katika makala.
gesi bora
Tunatambua mara moja kwamba fomula ya kasi ya wastani ya roboduara ya molekuli za gesi itatolewa mahususi kwa ajili ya gesi bora. Chini yake, katika fizikia, mfumo wa chembe nyingi huzingatiwa ambayo chembe (atomi, molekuli) haziingiliani na kila mmoja (nishati yao ya kinetic inazidi nishati inayowezekana ya mwingiliano na maagizo kadhaa ya ukubwa) na haina vipimo. Hiyo ni, ni pointi na molekuli finite (umbali kati ya chembe amri kadhaa ya ukubwa kubwa kuliko ukubwa wao.mstari).
Gesi yoyote ambayo ina molekuli au atomi zisizo na kemikali, na iliyo chini ya shinikizo la chini na joto la juu, inaweza kuchukuliwa kuwa bora. Kwa mfano, hewa ni gesi bora, lakini mvuke wa maji hauko hivyo tena (vifungo vikali vya hidrojeni hutenda kazi kati ya molekuli za maji).
Nadharia ya Kinetiki ya Molekuli (MKT)

Kusoma gesi bora ndani ya mfumo wa MKT, unapaswa kuzingatia michakato miwili muhimu:
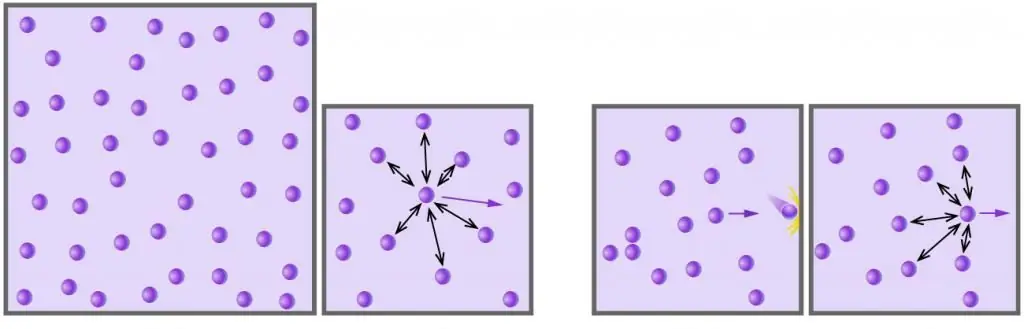
- Gesi huunda shinikizo kwa kuhamishia kwenye kuta za chombo kilicho ndani yake, kasi ambayo molekuli na atomi zinapogongana nazo. Migongano kama hii ni laini kabisa.
- Molekuli na atomi za gesi husogea bila mpangilio katika pande zote kwa kasi tofauti, ambayo usambazaji wake unatii takwimu za Maxwell-Boltzmann. Uwezekano wa mgongano kati ya chembechembe ni mdogo sana, kwa sababu ya ukubwa wao mdogo na umbali mkubwa kati yao.
Licha ya ukweli kwamba kasi ya mtu binafsi ya chembe za gesi ni tofauti sana kutoka kwa nyingine, thamani ya wastani ya thamani hii inabaki thabiti baada ya muda ikiwa hakuna athari za nje kwenye mfumo. Fomula ya wastani wa kasi ya mraba ya molekuli za gesi inaweza kupatikana kwa kuzingatia uhusiano kati ya nishati ya kinetiki na halijoto. Tutashughulikia suala hili katika aya inayofuata ya makala.
Utoaji wa fomula ya kasi ya wastani ya roboduara ya molekuli bora za gesi
Kila mwanafunzi anajua kutokana na kozi ya jumla ya fizikia kwamba nishati ya kinetiki ya mwendo wa kutafsiri wa mwili wenye uzito wa m huhesabiwa kama ifuatavyo:
Ek=mv2/2
V ni wapi kasi ya mstari. Kwa upande mwingine, nishati ya kinetiki ya chembe pia inaweza kubainishwa kulingana na halijoto kamili T, kwa kutumia kipengele cha ubadilishaji kB(Boltzmann's constant). Kwa kuwa nafasi yetu ni ya pande tatu, Ek inakokotolewa kama ifuatavyo:
Ek=3/2kBT.
Sawa na usawa na kuonyesha v kutoka kwao, tunapata fomula ya kasi ya wastani ya gesi bora ya quadratic:
mv2/2=3/2kBT=>
v=√(3kBT/m).
Katika fomula hii, m - ni wingi wa chembe ya gesi. Thamani yake si rahisi kutumia katika hesabu za vitendo, kwa kuwa ni ndogo (≈ 10-27kg). Ili kuepuka usumbufu huu, hebu tukumbuke uwiano wa gesi ya ulimwengu wote R na molekuli ya molar M. R isiyobadilika yenye kB inahusiana na usawa:
kB=R/NA.
Thamani ya M imefafanuliwa kama ifuatavyo:
M=mNA.
Kwa kuzingatia usawa zote mbili, tunapata usemi ufuatao wa kasi ya mzizi-maana-mraba ya molekuli:
v=√(3RT/M).
Kwa hivyo, wastani wa kasi ya mraba ya chembe za gesi inalingana moja kwa moja na mzizi wa mraba wa halijoto kamili na inawiana kinyume na mzizi wa mraba wa molekuli ya molar.
Mfano wa utatuzi wa matatizo
Kila mtu anajua kwamba hewa tunayopumua ni 99% ya nitrojeni na oksijeni. Ni muhimu kubainisha tofauti za kasi za wastani za molekuli N2 na O2 kwa joto la 15 o C.

Tatizo hili litatatuliwa kwa kufuatana. Kwanza, tunatafsiri halijoto kuwa vitengo kamili, tunayo:
T=273, 15 + 15=288, 15 K.
Sasa andika molekuli za molar kwa kila molekuli inayozingatiwa:
MN2=0.028 kg/mol;
MO2=0.032 kg/mol.
Kwa kuwa thamani za molekuli ya molar hutofautiana kidogo, kasi yao ya wastani katika halijoto sawa inapaswa pia kuwa karibu. Kwa kutumia fomula ya v, tunapata thamani zifuatazo za molekuli za nitrojeni na oksijeni:
v (N2)=√(38, 314288, 15/0, 028)=506.6 m/s;
v (O2)=√(38, 314288, 15/0, 032)=473.9 m/s.
Kwa sababu molekuli za nitrojeni ni nyepesi kidogo kuliko molekuli za oksijeni, huenda kwa kasi zaidi. Tofauti ya wastani ya kasi ni:
v (N2) - v (O2)=506.6 - 473.9=32.7 m/ s.
)
Thamani inayotokana ni 6.5% pekee ya kasi ya wastani ya molekuli za nitrojeni. Tunazingatia kasi ya juu ya molekuli katika gesi, hata katika halijoto ya chini.






