Njia ya uchanganuzi wa upitishaji ni kipimo cha upitishaji umeme wa kielektroniki ili kufuatilia maendeleo ya mmenyuko wa kemikali. Sayansi hii inatumika sana katika kemia ya uchanganuzi, ambapo titration ni njia ya kawaida ya kufanya kazi. conductometry ni nini? Katika mazoezi ya kawaida katika kemia ya uchanganuzi, neno hili hutumika kama kisawe cha titration, wakati pia hutumika kuelezea matumizi yasiyo ya titration. Je, ni faida gani ya kutumia mbinu hii ya uchanganuzi? Mara nyingi hutumika kubainisha utendakazi wa jumla wa suluhu au kuchanganua ncha ya titration inayohusisha ioni.
Historia
Vipimo tendaji vilianza mapema kama karne ya 18, wakati Andreas Baumgartner alipogundua kuwa maji ya chumvi na madini kutoka Bad Gastein hukoAustria inaendesha umeme. Kwa hivyo, matumizi ya njia hii kuamua usafi wa maji, ambayo hutumiwa mara nyingi leo kupima ufanisi wa mifumo ya utakaso wa maji, ilianza mnamo 1776. Ndivyo ilianza historia ya mbinu ya uchanganuzi ya kondakta.
Friedrich Kohlrausch aliendeleza maendeleo ya sayansi hii katika miaka ya 1860, alipotumia mkondo wa kupishana kwenye maji, asidi na miyeyusho mingine. Karibu na wakati huu, Willis Whitney, ambaye alikuwa akisoma mwingiliano wa asidi ya sulfuriki na chromium sulfate complexes, alipata mwisho wa kwanza wa conductometric. Matokeo haya yalifikia kilele cha titration ya potentiometri na chombo cha kwanza cha uchanganuzi wa ujazo na Robert Behrend mnamo 1883 katika titration ya kloridi na bromidi HgNO3. Kwa hivyo, mbinu ya kisasa ya uchanganuzi wa upitishaji unategemea Behrend.
Hatua hii ilifanya iwezekane kupima umumunyifu wa chumvi na ukolezi wa ioni za hidrojeni, pamoja na viwango vya asidi-msingi na redoksi. Njia ya uchanganuzi ya conductometric iliboreshwa na maendeleo ya electrode ya kioo, ambayo ilianza mwaka wa 1909.
Titration
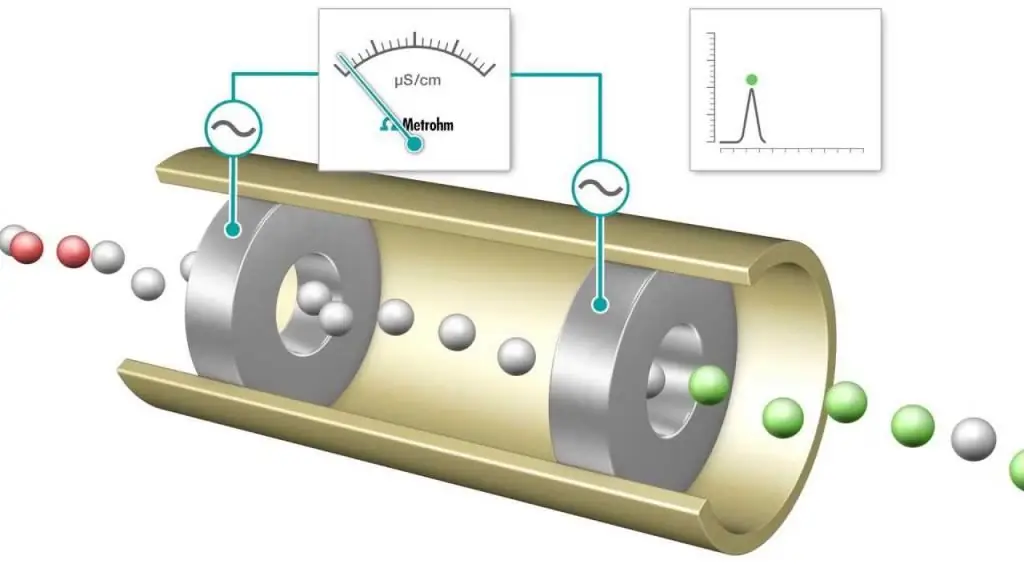
Titration ya Conductometric ni kipimo ambacho conductivity ya elektroliti ya mchanganyiko wa mmenyuko hufuatiliwa kila mara kwa kuongeza kitendanishi kimoja. Hatua ya usawa ni hatua ambayo conductivity inabadilika ghafla. Ongezeko linaloonekana au kupungua kwa conductivity kunahusishwa na mabadiliko katika mkusanyiko wa ioni mbili za conductive zaidi, hidrojeni na hidroksidi. Mbinu hiiinaweza kutumika kurekebisha miyeyusho ya rangi au kusimamishwa kwa usawa (k.m. kusimamishwa kwa massa ya mbao) ambayo haiwezi kutumika na viashirio vya kawaida.
Uainishaji wa asidi-asidi na redoksi mara nyingi hufanywa, ambayo hutumia viashirio vya kawaida kubainisha sehemu ya mwisho, kama vile methyl chungwa, phenolphthalein kwa titration-msingi ya asidi, na miyeyusho ya wanga kwa mchakato wa redoksi wa aina ya iodometric. Hata hivyo, vipimo vya upitishaji umeme vinaweza pia kutumika kama zana ya kubainisha mahali pa mwisho, kwa mfano wakati wa kuangalia myeyusho wa HCl wenye msingi thabiti wa NaOH.
Ubadilishaji wa protoni
Titration inapoendelea, protoni hutenganishwa na kuunda NaOH kwa kutengeneza maji. Kwa kila kiasi cha NaOH kinachoongezwa, idadi sawa ya ioni za hidrojeni huondolewa. Kwa kweli, cation ya simu ya H + inabadilishwa na ion ya Na + ya chini ya simu, na conductivity ya ufumbuzi wa titrated, pamoja na conductivity ya seli iliyopimwa, kupungua. Hii inaendelea hadi hatua ya usawa inafikiwa ambapo suluhisho la kloridi ya sodiamu NaCl inaweza kupatikana. Msingi zaidi ukiongezwa, kuna ongezeko kadiri Na+ na OH- ioni zaidi zinapoongezwa na athari ya kutoweka haiondoi tena kiwango kinachokubalika cha H+.

Kwa hivyo, asidi kali inapowekwa alama kwa besi thabiti, utendishaji huwa na kiwango cha chini zaidi katika sehemu ya usawa. Kiwango cha chini hikiinaweza kutumika badala ya rangi ya kiashirio ili kuamua mwisho wa titration. Curve ya titration ni grafu ya maadili yaliyopimwa ya conductivity au conductivity kama kipengele cha kiasi cha ufumbuzi wa NaOH ulioongezwa. Mviringo wa titration unaweza kutumika kubainisha kielelezo sehemu ya usawa. Mbinu ya uchanganuzi ya upitishaji (na matumizi yake) inafaa sana katika kemia ya kisasa.
Maoni
Kwa majibu kati ya besi dhaifu ya asidi-dhaifu, upitishaji wa umeme hupungua kwanza kwa kiasi, kwa kuwa ioni chache za H+ zinazopatikana hutumiwa. Kisha conductivity huongezeka kidogo hadi kiasi cha hatua ya usawa kutokana na mchango wa cation ya chumvi na anion (mchango huu katika kesi ya msingi wa asidi kali hauzingatiwi na hauzingatiwi huko.) Baada ya hatua ya usawa kufikiwa., mdundo huongezeka kwa kasi kutokana na ziada ya ioni za OH.
Vigunduzi vya upitishaji (mbinu ya uchanganuzi pitiota) pia hutumika kupima viwango vya elektroliti katika miyeyusho yenye maji. Mkusanyiko wa molar wa kichanganuzi unaounda upitishaji wa myeyusho unaweza kupatikana kutoka kwa kipimo cha upinzani cha umeme cha mmumuko.
Mbinu ya conductometric ya uchanganuzi: kanuni na fomula
(2.4.13) C=Constcell1Λm1Res, ambapo Constcell ni thamani ya kudumu kulingana na seli ya kupimia, Res ni upinzani wa umeme unaopimwa na kifaa (kulingana na sheria ya Ohm Res=I / V, na kwa mara kwa mara Ukubwa wa kipimo cha voltage V I hukuruhusu kukokotoa Res), na Λm ni sawaconductivity kwa chembe ionic. Ingawa kwa madhumuni ya vitendo Λm inaweza kuzingatiwa mara kwa mara, inategemea umakini kulingana na sheria ya Kohlrausch:
(2.4.14)=Хт Λm0-ΘC, ambapo Θ ni thabiti, na Λm0 ni sifa inayozuia upitishaji wa molar ya kila ayoni. Mwendo wa molar, kwa upande wake, hutegemea halijoto.
Maandishi
Uundaji wa mbinu ya upitishaji vipimo vya uchanganuzi wa vipimo umewafanya wanasayansi kugundua uvumbuzi mpya. Wanasayansi waliamua uwiano muhimu wa upenyezaji wa juu zaidi, Scrit, kwa kutumia conductometry katika mfumo wa hali ya hewa wa AgCl unaozidi ioni za Ag+, kwa kutumia hidrolisisi ya kloridi ya alkili kama chanzo cha ioni za CI. Walipata Scrit=1.51, 1.73 na 1.85 saa 15, 25 na 35°C mtawalia, ambapo S=([Ag+][Cl-] / Ksp) 1/2 kwa ufafanuzi wao. Ufafanuzi huu wa kipengele cha kueneza zaidi utabadilishwa kuwa wetu (S=[Ag+][Cl-] / Ksp), matokeo ni 2.28, 2.99 na 3.42, mtawalia, kwa makubaliano mazuri na matokeo ya utafiti huu. Hata hivyo, utegemezi wa joto wa Scrit ni kinyume na ule ulioelezwa katika utafiti huu. Ingawa sababu ya mkanganyiko huu haijulikani wazi, kupungua kwa Maandishi na joto linaloongezeka kunaweza kuwa sawa, kwani kiwango cha nucleation kinabadilika sana na mabadiliko madogo katika ΔGm/ kT, na kwa hivyo ΔGm/ kT, ambayo ni sawia na T. − 3 (lnSm) 2 kulingana na fomula (1.4.12) inachukuliwa kuwa karibu mara kwa mara na mabadiliko ya joto katika mfumo uliopewa. Kwa bahati mbaya, ufafanuzi wa S lazima uwe [Ag +] [Cl -] / Ksp, kwa kuwa uwiano wa kueneza zaidi katika suala la[AgCl] ukolezi wa monoma mwanzoni ulitolewa kama S=[AgCl] / [AgCl] (∞)=[Ag +] [Cl -] / Ksp.
Tanaka and Iwasaki
Historia ya mbinu dhabiti ya uchanganuzi iliendelea na wanasayansi wawili mashuhuri wa Kijapani. Tanaka na Iwasaki walisoma mchakato wa uundaji wa chembe za AgCl na AgBr kwa kutumia njia ya mtiririko uliosimamishwa pamoja na spectrophotometer ya chaneli nyingi, ambayo ni muhimu kwa kusoma mchakato wa haraka kwa mpangilio wa msec. Waligundua kuwa aina fulani maalum ya halidi ya fedha AgXm (m-1), ikiwa na mkanda mwembamba wa kunyonya UV, iliundwa papo hapo wakati suluhisho la AgC104 la mpangilio wa 10-4 mol dm-3 lilipochanganywa na KX (X=Cl au Br) suluhisho la mpangilio wa kutoka 10-2 hadi 10-1 mol dm-3 ikifuatiwa na kuoza kwake haraka kwa takriban 10 ms na kuunda bidhaa ya kati iliyo na unyonyaji mpana wa UV na mabadiliko polepole zaidi katika wigo. ya bidhaa ya kati. Walifasiri ya kati kama chembe za monodisperse (AgX) n inayojumuisha n molekuli na kuamuliwa n kutoka kwa uwiano unaoonekana -dC/dt α Cn kwa t=0 kwa viwango mbalimbali vya awali vya C precursor AgXm (m-1) - (n=7 -10 kwa AgCl, n=3-4 kwa AgBr).

Hata hivyo, kwa kuwa kianzilishi AgXm (m − 1) huharibika kwa njia isiyo ya kusimama, nadharia ya nukleo ya quasi-stationary haitumiki katika mchakato huu, na kwa hivyo thamani inayotokana ya n hailingani na nthamani ya viini muhimu. Ikiwa bidhaa ya kati ina viini vya monodisperse n,inayoundwa na changamano cha monomeriki, uwiano wa -dC/dt α C hauwezi kudumishwa. Isipokuwa tukichukulia kuwa vishada vidogo kuliko n-mers viko katika usawa, ki − 1, ici − 1c1=ki, i - 1ci, na kila kimoja katika mmenyuko mfuatano c1 → c2 → c3 →… → cn − 1 → cn., na hatua ya mwisho tu cn − 1 → cn haiwezi kutenduliwa; yaani c1⇌c2⇌c3⇌… ⇌cn − 1 → cn.
Mbali na hilo, inafaa kudhaniwa kuwa viwango vya vishada kutoka 2 hadi n-1 vina viwango vya usawa vya kupuuza. Walakini, inaonekana hakuna msingi wa kuhalalisha mawazo haya. Kwa upande mwingine, tulijaribu kuhesabu radii ya nuclei muhimu na coefficients ya supersaturation S mwishoni mwa mchakato wa haraka, kwa kutumia γ=101 mJ m - 2 kwa cubic AgCl19 na γ=109 mJ m - 2 kwa cubic AgBr20, kwa kuchukulia kuwa thamani za n, 7-10 za AgCl19 na 3-4 za AgBr20, ni sawa na saizi ya viini vya monodisperse, n. Mbinu ya uchanganuzi wa upitishaji, hakiki ambazo huanzia kuidhinisha hadi kuvutiwa, zilileta kuzaliwa upya kwa kemia kama sayansi.
Kutokana na hilo, wanasayansi waligundua fomula ifuatayo: r=0.451 nm na S=105 kwa AgCl yenye n=9; r=0.358 nm na S=1230 kwa AgBr na n=4. Kwa kuwa mifumo yao inalinganishwa na ile ya Davis na Jones, ambayo ilipata supersaturation muhimu ya AgCl ya karibu 1.7-2.0 saa 25 ° C. Kwa kutumia kondometa ya mchanganyiko wa moja kwa moja katika viwango sawa vya miyeyusho ya maji iliyoyeyushwa ya AgNO3 na KCl, thamani za juu zaidi za S huenda zisionyeshe vipengele halisi vya kujaa kupita kiasi.katika usawa na viini vya kati.
ufyonzaji wa UV
Inaonekana ni jambo la busara zaidi kuhusisha ufyonzwaji wa kati wenye mpana wa UV kwa viini vikubwa zaidi kuliko wastani na mgawanyo wa saizi pana unaotokana na mmenyuko usio wa kusimama uliosimama. Mabadiliko ya polepole yaliyofuata ya viini vya kati inaonekana kuwa yanahusiana na kukomaa kwao huko Ostwald.

Katika muktadha ulio hapo juu, mwanakemia wa Kiamerika Nielsen pia alipata nsawa na 12 na S inayolingana zaidi ya 103 kwa upanuzi wa chembe za salfati ya bariamu kutokana na vipimo vya tope kama kazi ya kueneza kupita kiasi, kwa kutumia n=dlogJ / dlogC katika nadharia ya Becher-Dering-kama kwa fomula. (1.3.37), lakini kutoa (n+ 1) badala ya n. Kwa kuwa miyeyusho ya ioni za bariamu na ioni za salfati zilichanganywa moja kwa moja katika jaribio hili, nuklea ya haraka ya muda mfupi inapaswa kumalizika mara baada ya kuchanganywa, na kilichopimwa kinaweza kuwa kasi ya upevushaji wa polepole uliofuata wa Ostwald na/au muunganisho wa viini vilivyozalishwa. Inavyoonekana, hii ndiyo sababu ya thamani ndogo isiyo na sababu ya n na ujazo wa juu sana. Kwa hiyo, ni lazima tena kutambua kwamba baadhi ya hifadhi ya aina monomeric kwamba releases yao katika kukabiliana na matumizi yao daima ni muhimu kufikia nucleation quasi-stationary katika mfumo funge. Nadharia zote za kitamaduni za uhuishaji, pamoja na nadharia ya Becher-Döring, huchukulia hali kama hiyo kwa udhahiri. Ufafanuzi wa conductometricnjia ya uchambuzi ilitolewa katika sehemu za makala hapo juu.
kutoka 4 ns hadi 3 μs. Muonekano wa bidhaa hizo ulirekodiwa kwa kutumia picha ya kuzidisha picha na kamera ya mfululizo na vitangulizi vya halidi vya fedha vya monomeriki vilipatikana kuunda kwa muda kwa mpangilio wa sekunde ndogo na kufuatiwa na mchakato wa nukleo sawa na ule uliozingatiwa na Tanaka na Iwasaki. Matokeo yao yanaonyesha wazi kwamba mchakato wa nucleation ya halidi za fedha kwa kuchanganya moja kwa moja ya reactants lina hatua mbili za msingi; yaani, uundaji wa mtangulizi wa monomeric wa utaratibu wa μs na mabadiliko ya baadae kwa nuclei ya utaratibu wa 10 ms. Ikumbukwe kwamba ukubwa wa wastani wa viini ni takriban nm 10.
Kueneza
Kuhusu viambajengo vya kueneza kwa wingi kwa viini vya chembechembe za AgCl katika mifumo iliyofunguliwa ambapo viwango vya juu vya viitikio kama vile AgNO3 na KCl huletwa kwa mfululizo kwenye myeyusho wa gelatin wakati wote wa mvua, Strong na Wey31 ziliripoti 1.029 (80° C) - 1.260 (40°C) na Leubner32 ziliripoti 1.024 katika 60°C kama ilivyokadiriwa kutokana na kupima kasi ya ukuaji wa chembechembe za mbegu za AgCl katika hali ya kuzidisha sana. Hiki ndicho kiini cha mbinu ya upitishaji ya uchanganuzi wa kiasi.
Kwa upande mwingine, kwa mifumo iliyofunguliwa ya chembe za AgBr, baadhimakadirio ya maadili ya mgawo muhimu wa ueneaji zaidi, Scrit: Scrit∼-1.5 kwa 70 °C kulingana na Wey na Strong33 kutoka kwa kiwango cha juu cha ukuaji kinachotegemea saizi kinachoamuliwa kwa kupata kizingiti cha kurudisha nyuma kwa viwango tofauti vya kuongeza suluhisho la AgNO3 kwa KBr. suluhisho mbele ya chembe za mbegu na jets mbili; Scrit=1.2-1.5 kwa 25°C kulingana na Jagannathan na Wey34 kama kipengele cha juu zaidi cha kujaa kupita kiasi kilichobainishwa kutoka kwa mlingano wa Gibbs-Thomson na data yao kuhusu ukubwa wa chini wa wastani wa viini unaozingatiwa na hadubini ya elektroni wakati wa hatua ya unyukliaji wa mvua ya ndege mbili za AgBr.. Hii ni nzuri sana wakati wa kutumia mbinu ya upimaji kondakta.

Wakati wa kukokotoa maadili haya ya Scrit, walichukua γ=140 mJ m − 2. Kwa kuwa nukleo katika mifumo iliyo wazi inalingana na mchakato wa kuishi kwa viini vilivyochanga vilivyoundwa katika eneo la ndani la ujazo wa juu sana karibu na maduka ya kiitikio, muhimu sana. kueneza kupita kiasi kunalingana na mkusanyiko wa soluti katika usawa na viini vya ukubwa wa juu zaidi, ikiwa tunatumia data ya Sugimoto35 kwenye upeo wa juu wa radius ya viini vya AgBr katika mifumo iliyo wazi (.3 8.3 nm) yenye γ ya kinadharia kwa ujazo wa AgBr (=109 mJ m − 2)) 3, kisha kipengele muhimu cha kueneza kupita kiasi, Scrit, kinakokotolewa kama ingekuwa 1.36 kwa 25°C (ikiwa γ inachukuliwa kuwa 140 mJ/m2, basi Scrit=1.48).
Kwa hivyo, kwa vyovyote vile, mienendo mikuu muhimu katikamifumo iliyo wazi ya chembe za halidi ya fedha kwa kawaida huwa chini ya kiwango cha juu zaidi (pengine karibu na mienendo muhimu zaidi) katika mifumo iliyofungwa. Hii ni kwa sababu wastani wa eneo la viini vinavyozalishwa katika eneo la ndani la mfumo wazi ni kubwa zaidi kuliko rmkatika mfumo uliofungwa, labda kwa sababu ya muunganisho wa papo hapo wa viini vya msingi vilivyojilimbikizia sana katika ukanda wa ndani wa mfumo wazi na wa juu. ukolezi wa elektroliti ndani.
Maombi
Matumizi ya mbinu ya uwekaji titometriki kwa kurekodi mfululizo wakati wa michakato ya enzymatic yamechunguzwa na kuchambuliwa kwa kina. Takriban mbinu zote za uchanganuzi za kielektroniki zinatokana na athari za kielektroniki (potentiometry, voltammetry, amperometry, coulometry).
Njia ya uchanganuzi wa upitishaji ni mbinu ambayo ama hakuna miitikio ya kielektroniki kwenye elektrodi kabisa, au kuna miitikio ya pili inayoweza kupuuzwa. Kwa hivyo, katika njia hii, mali muhimu zaidi ya suluhisho la elektroliti kwenye safu ya mpaka ni upitishaji wake wa umeme, ambao hutofautiana kulingana na anuwai ya athari za kibaolojia.
Faida
Vitambuzi vya kibayolojia vya Conductometric pia vina manufaa fulani juu ya aina nyingine za vibadilishaji data. Kwanza, zinaweza kufanywa kwa kutumia teknolojia ya kiwango cha filamu nyembamba ya gharama nafuu. Hii, pamoja na utumiaji wa njia iliyoboreshwa ya kuweka nyenzo za kibaolojia, husababisha kupunguzwa kwa gharama ya msingi ya vifaa na.gharama ya jumla ya uchambuzi. Kwa vitambua vijiumbe vilivyojengewa ndani, ni rahisi kutekeleza hali ya kipimo tofauti, ambayo hulipa fidia kwa athari za nje na kuboresha kwa kiasi kikubwa usahihi wa kipimo.
Data inaonyesha kwa uwazi uwezo mkubwa wa vitambuzi vya kibaolojia kondakta. Hata hivyo, hii bado ni mwelekeo mpya kabisa katika vitambuzi, kwa hivyo uundaji wa vifaa vya kibiashara una mustakabali mzuri.
Njia mpya
Baadhi ya wanasayansi wameelezea mbinu ya jumla ya kupima pKa kwa utendakazi. Njia hii ilitumiwa sana hadi mwaka wa 1932 (kabla ya mbinu za kupima pH kutumika). Mbinu ya upitishaji ni nyeti sana kwa halijoto na haiwezi kutumika kupima thamani za pKa zinazopishana. Faida inayowezekana kwa sampuli bila chromophore ni kwamba inaweza kutumika katika suluhisho la dilute sana, hadi 2.8 × 10-5 M. Katika miaka ya hivi karibuni, conductometry 87 imetumika kupima pKa ya lidocaine, ingawa matokeo yaliyopatikana yalikuwa 0.7 kwa kila kitengo chini ya thamani ya pH inayokubalika kwa ujumla.

Albert na Sajini pia walielezea mbinu ya kubainisha pKa kutokana na vipimo vya umumunyifu. Kama ilivyoelezwa hapo juu, umumunyifu hutegemea pKa, kwa hivyo ikiwa umumunyifu unapimwa kwa thamani nyingi za pH kwenye curve, pKa inaweza kubainishwa. Peck na Benet walieleza mbinu ya jumla ya kukadiria thamani za pKa kwa dutu moja, diprotic, na amphoteric kutokana na seti ya umumunyifu na vipimo vya pH. Hansen na Hafliger walipata pKa ya sampuli, ambayohutengana haraka kwa hidrolisisi kutoka viwango vyake vya awali vya kufutwa kama utendaji wa pH katika kifaa cha diski kinachozunguka. Matokeo yanakubaliana vyema na matokeo ya pH/UV, lakini mtengano hufanya njia ya mwisho kuwa ngumu. Haya ni, kwa kiasi kikubwa, maelezo ya mbinu ya uchanganuzi kondakta.






