Maarifa ya fasili katika fizikia ni jambo kuu la kutatua kwa mafanikio matatizo mbalimbali ya kimwili. Katika makala haya, tutazingatia maana ya michakato ya isobaric, isochoric, isothermal na adiabatic kwa mfumo bora wa gesi.
Gesi bora na mlingano wake
Kabla ya kuendelea na maelezo ya michakato ya isobariki, isokororiki na isothermal, hebu tuzingatie gesi bora ni nini. Chini ya ufafanuzi huu katika fizikia wanazingatia mfumo unaojumuisha idadi kubwa ya chembe zisizo na kipimo na zisizoingiliana ambazo husogea kwa kasi kubwa katika pande zote. Kwa kweli, tunazungumza juu ya hali ya jumla ya gesi, ambayo umbali kati ya atomi na molekuli huzidi saizi zao na ambayo nishati inayowezekana ya mwingiliano wa chembe hupuuzwa kwa sababu ya udogo wake, ikilinganishwa na nishati ya kinetic.
Hali ya gesi bora ni jumla ya vigezo vyake vya halijoto. Ya kuu ni joto, kiasi na shinikizo. Wacha tuwaeleze kwa herufi T, V na P, mtawaliwa. Katika miaka ya 30 ya karne ya XIXClapeyron (mwanasayansi wa Ufaransa) aliandika kwanza mlinganyo unaochanganya vigezo vya halijoto vilivyoonyeshwa ndani ya usawa mmoja. Inaonekana kama:
PV=nRT,
ambapo n na R ni wingi wa dutu na gesi isiyobadilika, mtawalia.
Isoprocesses katika gesi ni nini?
Kama wengi wameona, michakato ya isobaric, isochoric na isothermal hutumia kiambishi sawa cha "iso" katika majina yao. Inamaanisha usawa wa parameter moja ya thermodynamic wakati wa kifungu cha mchakato mzima, wakati vigezo vilivyobaki vinabadilika. Kwa mfano, mchakato wa isothermal unaonyesha kwamba, kwa sababu hiyo, joto kamili la mfumo hudumishwa mara kwa mara, wakati mchakato wa isochoric unaonyesha kiasi cha mara kwa mara.
Isoprocesses ni rahisi kusoma, kwa kuwa kurekebisha moja ya vigezo vya thermodynamic husababisha kurahisisha mlinganyo wa jumla wa hali ya gesi. Ni muhimu kutambua kwamba sheria za gesi za isoprocesses hizi zote ziligunduliwa kwa majaribio. Uchanganuzi wao ulimruhusu Clapeyron kupata mlingano wa jumla uliopunguzwa.
Isobaric, isochoric na isothermal michakato
Sheria ya kwanza iligunduliwa kwa mchakato wa isothermal katika gesi bora. Sasa inaitwa sheria ya Boyle-Mariotte. Kwa kuwa T haibadiliki, mlinganyo wa hali unamaanisha usawa:
PV=const.
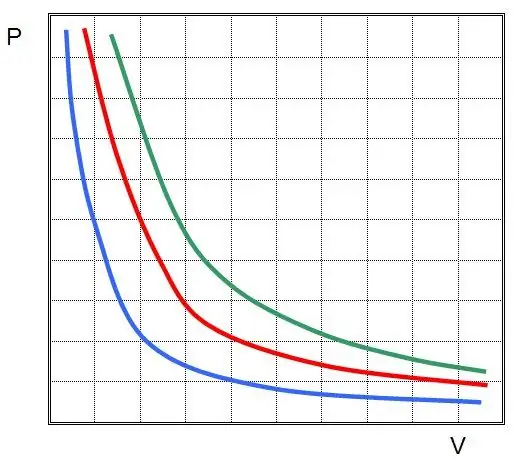
Kwa maneno mengine, mabadiliko yoyote ya shinikizo katika mfumo husababisha mabadiliko ya sawia katika ujazo wake, ikiwa halijoto ya gesi itadumishwa bila kubadilika. Grafu ya chaguo za kukokotoa P(V) nihyperbole.
Mchakato wa Isobaric - hii ni badiliko katika hali ya mfumo, ambapo shinikizo hubaki thabiti. Baada ya kuweka thamani ya P katika mlinganyo wa Clapeyron, tunapata sheria ifuatayo:
V/T=const.
Usawa huu una jina la mwanafizikia Mfaransa Jacques Charles, aliyeupokea mwishoni mwa karne ya 18. Isobar (uwakilishi wa picha wa kazi ya V(T) inaonekana kama mstari ulionyooka. Kadiri shinikizo linavyoongezeka kwenye mfumo, ndivyo laini hii inavyopanda kwa kasi zaidi.
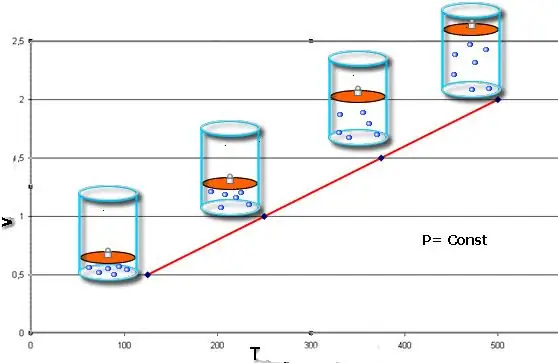
Mchakato wa isobaric ni rahisi kutekelezwa ikiwa gesi itapashwa joto chini ya pistoni. Molekuli za mwisho huongeza kasi yao (nishati ya kinetic), huunda shinikizo la juu kwenye pistoni, ambayo inaongoza kwa upanuzi wa gesi na kudumisha thamani ya mara kwa mara ya P.
Mwishowe, mchakato wa tatu ni isochoric. Inaendesha kwa kiasi cha mara kwa mara. Kutoka kwa mlinganyo wa hali tunapata usawa unaolingana:
P/T=const.
Inajulikana miongoni mwa wanafizikia kama sheria ya Gay-Lussac. Uwiano wa moja kwa moja kati ya shinikizo na halijoto kamili unaonyesha kwamba grafu ya mchakato wa isokororiki, kama grafu ya isobari, ni mstari ulionyooka wenye mteremko chanya.
Ni muhimu kuelewa kwamba isoprocesses zote hutokea katika mifumo iliyofungwa, yaani, thamani ya n huhifadhiwa wakati wa mwendo wao.
Mchakato wa Adiabatic
Mchakato huu haumo katika kategoria ya "iso", kwa kuwa vigezo vyote vitatu vya halijoto hubadilika wakati wa kupitisha. adiabaticinayoitwa mpito kati ya majimbo mawili ya mfumo, ambayo haina kubadilishana joto na mazingira. Kwa hivyo, upanuzi wa mfumo unafanywa kutokana na hifadhi yake ya ndani ya nishati, ambayo husababisha kushuka kwa kiasi kikubwa kwa shinikizo na joto kamili ndani yake.
Mchakato wa adiabatic kwa gesi bora unafafanuliwa na milinganyo ya Poisson. Mmoja wao ameonyeshwa hapa chini:
PVγ=const,
ambapo γ ni uwiano wa uwezo wa joto katika shinikizo la mara kwa mara na kwa sauti isiyobadilika.
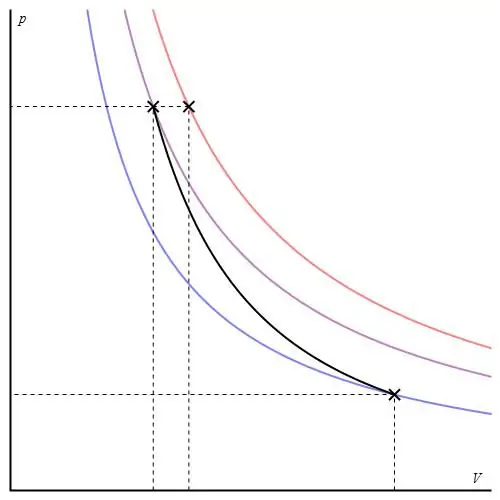
Grafu ya adiabatiki inatofautiana na grafu ya mchakato wa isochoriki na grafu ya isobariki, lakini inafanana na haipabola (isotherm). Adiabat katika shoka za P-V hufanya kazi kwa ukali zaidi kuliko isotherm.






