Ulimwengu tunamoishi ni mzuri mno na umejaa michakato mingi tofauti inayoweka mkondo wa maisha. Taratibu hizi zote zinasomwa na sayansi inayojulikana - fizikia. Inatoa fursa ya kupata angalau wazo fulani la asili ya ulimwengu. Katika nakala hii, tutazingatia dhana kama nadharia ya kinetic ya Masi, hesabu zake, aina na fomula. Hata hivyo, kabla ya kuendelea na uchunguzi wa kina wa masuala haya, unahitaji kufafanua mwenyewe maana halisi ya fizikia na maeneo inayosoma.
Fizikia ni nini?

Kwa kweli, hii ni sayansi pana sana na, pengine, mojawapo ya msingi zaidi katika historia ya wanadamu. Kwa mfano, ikiwa sayansi hiyo hiyo ya kompyuta inahusishwa na karibu kila eneo la shughuli za binadamu, iwe ni muundo wa computational au uundaji wa katuni, basi fizikia ni maisha yenyewe, maelezo ya michakato yake ngumu na mtiririko. Hebu tujaribu kubainisha maana yake, na kurahisisha uelewa wetu kadri tuwezavyo.
Kwa hiyoKwa hiyo, fizikia ni sayansi inayohusika na utafiti wa nishati na jambo, uhusiano kati yao, maelezo ya michakato mingi inayotokea katika ulimwengu wetu mkubwa. Nadharia ya molekuli-kinetic ya muundo wa maada ni tone dogo tu katika bahari ya nadharia na matawi ya fizikia.
Nishati, ambayo sayansi hii inachunguza kwa kina, inaweza kuwakilishwa katika aina mbalimbali. Kwa mfano, kwa namna ya mwanga, mwendo, mvuto, mionzi, umeme na aina nyingine nyingi. Tutagusia katika makala haya nadharia ya kinetiki ya molekuli ya muundo wa maumbo haya.
Utafiti wa maada hutupatia wazo la muundo wa atomiki wa maada. Kwa njia, inafuata kutoka kwa nadharia ya Masi-kinetic. Sayansi ya muundo wa maada inatuwezesha kuelewa na kupata maana ya kuwepo kwetu, sababu za kutokea kwa uhai na Ulimwengu wenyewe. Hebu bado tujaribu kusoma nadharia ya kinetiki ya molekuli ya jambo.
Kwanza, baadhi ya utangulizi unahitajika ili kuelewa kikamilifu istilahi na hitimisho lolote.
Mada ya Fizikia
Tukijibu swali la nadharia ya molekuli-kinetiki ni nini, mtu hawezi ila kuzungumzia sehemu za fizikia. Kila moja ya haya inahusika na uchunguzi wa kina na maelezo ya eneo fulani la maisha ya mwanadamu. Zimeainishwa kama ifuatavyo:
- Mekaniki, ambayo imegawanywa katika sehemu mbili zaidi: kinematiki na mienendo.
- Tuli.
- Thermodynamics.
- sehemu ya molekuli.
- Electrodynamics.
- Optics.
- Fizikia ya quantumu na kiini cha atomiki.
Wacha tuzungumze haswa kuhusu molekulifizikia, kwa sababu inategemea nadharia ya molekuli-kinetiki.
Thermodynamics ni nini?
Kwa ujumla, sehemu ya molekuli na thermodynamics ni matawi yanayohusiana kwa karibu ya fizikia, ambayo huchunguza kwa upekee sehemu ya jumla ya idadi ya mifumo halisi. Inafaa kukumbuka kuwa sayansi hizi zinaelezea kwa usahihi hali ya ndani ya miili na vitu. Kwa mfano, hali yao wakati wa joto, fuwele, vaporization na condensation, katika ngazi ya atomiki. Kwa maneno mengine, fizikia ya molekuli ni sayansi ya mifumo inayojumuisha idadi kubwa ya chembe: atomi na molekuli.
Ni sayansi hizi zilizosoma masharti makuu ya nadharia ya kinetiki ya molekuli.
Hata katika darasa la saba, tulifahamiana na dhana za ulimwengu mdogo na mkubwa, mifumo. Haitakuwa jambo la ziada kuonyesha upya masharti haya kwenye kumbukumbu.
Dunia ndogo, kama tunavyoweza kuona kutoka kwa jina lake yenyewe, imeundwa na chembe za msingi. Kwa maneno mengine, huu ni ulimwengu wa chembe ndogo. Ukubwa wao hupimwa katika safu kutoka 10-18 m hadi 10-4 m, na wakati wa hali yao halisi unaweza kufikia infinity na vipindi vidogo visivyo na uwiano, kwa mfano, 10-20 s.
Macroworld inazingatia miili na mifumo ya umbo thabiti, inayojumuisha chembe nyingi za msingi. Mifumo kama hii inalingana na saizi yetu ya kibinadamu.
Kwa kuongeza, kuna kitu kama ulimwengu mkubwa. Inaundwa na sayari kubwa, galaksi za ulimwengu na tata.
Misinginadharia
Kwa kuwa sasa tumerejea kidogo na kukumbuka masharti ya kimsingi ya fizikia, tunaweza kwenda moja kwa moja kwenye mada kuu ya makala haya.
Nadharia ya Molekuli-kinetiki ilionekana na iliundwa kwa mara ya kwanza katika karne ya kumi na tisa. Kiini chake kiko katika ukweli kwamba inaelezea kwa undani muundo wa dutu yoyote (mara nyingi zaidi muundo wa gesi kuliko miili dhabiti na kioevu), kwa kuzingatia vifungu vitatu vya kimsingi ambavyo vilikusanywa kutoka kwa mawazo ya wanasayansi mashuhuri kama Robert Hooke, Isaac. Newton, Daniel Bernoulli, Mikhail Lomonosov na wengine wengi.
Vifungu vikuu vya nadharia ya kinetiki ya molekuli vinasikika kama hii:
- Hakika dutu zote (bila kujali ni kioevu, kigumu au gesi) zina muundo changamano, unaojumuisha chembe ndogo zaidi: molekuli na atomi. Wakati fulani atomi huitwa "molekuli za msingi".
- Chembechembe hizi zote za msingi huwa katika hali ya msogeo unaoendelea na wa fujo. Kila mmoja wetu amepata uthibitisho wa moja kwa moja wa pendekezo hili, lakini, uwezekano mkubwa, hakuwa na umuhimu mkubwa kwake. Kwa mfano, sote tuliona dhidi ya usuli wa miale ya jua kwamba chembe za vumbi zinasonga kila mara katika mwelekeo wenye machafuko. Hii ni kwa sababu ya ukweli kwamba atomi hutoa msukumo wa pande zote kwa kila mmoja, zikitoa nishati ya kinetic kila wakati kwa kila mmoja. Jambo hili lilichunguzwa kwa mara ya kwanza mnamo 1827, na lilipewa jina la mgunduzi - "mwendo wa Brown".
- Chembechembe zote za msingi ziko katika mchakato wa mwingiliano unaoendelea nanguvu fulani ambazo zina mwamba wa umeme.
Inafaa kuzingatia kwamba mfano mwingine unaoelezea nafasi nambari mbili, ambayo inaweza pia kutumika, kwa mfano, kwa nadharia ya kinetiki ya molekuli ya gesi, ni mgawanyiko. Tunakumbana nayo katika maisha ya kila siku, na katika majaribio na vidhibiti vingi, kwa hivyo ni muhimu kuwa na wazo kuihusu.
Kwanza, zingatia mifano ifuatayo:
Daktari alimwaga pombe kwa bahati mbaya kutoka kwenye chupa kwenye meza. Au labda ulidondosha chupa yako ya manukato na kuenea sakafuni.
Kwa nini, katika matukio haya mawili, harufu ya pombe na harufu ya manukato itajaa chumba kizima baada ya muda fulani, na sio tu eneo ambalo yaliyomo ya vitu hivi vilimwagika?
Jibu ni rahisi: diffusion.
Diffusion - ni nini? Je, inatiririka vipi?

Huu ni mchakato ambapo chembe zinazounda dutu fulani (kawaida gesi) hupenya ndani ya tupu za kati ya molekuli za nyingine. Katika mifano yetu hapo juu, yafuatayo yalitokea: kwa sababu ya joto, ambayo ni, harakati inayoendelea na iliyotenganishwa, molekuli za pombe na / au manukato zilianguka kwenye mapengo kati ya molekuli za hewa. Hatua kwa hatua, chini ya ushawishi wa mgongano na atomi na molekuli za hewa, huenea kuzunguka chumba. Kwa njia, ukubwa wa uenezi, yaani, kasi ya mtiririko wake, inategemea wiani wa vitu vinavyohusika katika kuenea, na pia juu ya nishati ya mwendo wa atomi zao na molekuli, inayoitwa kinetic. Kadiri nishati ya kinetiki inavyokuwa kubwa, ndivyo kasi ya molekuli hizi inavyoongezeka, mtawalia, na ukali.
Mchakato wa kasi wa usambaaji unaweza kuitwa usambaaji katika gesi. Hii ni kutokana na ukweli kwamba gesi haina homogeneous katika muundo wake, ambayo ina maana kwamba voids intermolecular katika gesi huchukua kiasi kikubwa cha nafasi, kwa mtiririko huo, na mchakato wa kupata atomi na molekuli ya dutu ya kigeni ndani yao unaendelea kwa urahisi na kwa kasi..
Mchakato huu ni polepole zaidi katika vimiminiko. Kuyeyushwa kwa vipande vya sukari kwenye kikombe cha chai ni mfano tu wa usambaaji wa kigumu kwenye kimiminika.
Lakini muda mrefu zaidi ni mtawanyiko katika miili yenye muundo thabiti wa fuwele. Hii ni hivyo hasa, kwa sababu muundo wa yabisi ni homogeneous na ina kimiani yenye nguvu ya kioo, katika seli ambazo atomi za vibrate imara. Kwa mfano, ikiwa nyuso za baa mbili za chuma zimesafishwa vizuri na kisha kugusana, basi baada ya muda mrefu wa kutosha tutaweza kugundua vipande vya chuma kimoja katika nyingine, na kinyume chake.
Kama sehemu nyingine yoyote ya msingi, nadharia ya msingi ya fizikia imegawanywa katika sehemu tofauti: uainishaji, aina, fomula, milinganyo, na kadhalika. Hivyo, tumejifunza misingi ya nadharia ya kinetiki ya molekuli. Hii inamaanisha kuwa unaweza kuendelea kwa usalama kwa kuzingatia vizuizi mahususi vya kinadharia.
Nadharia ya Molekuli-kinetiki ya gesi
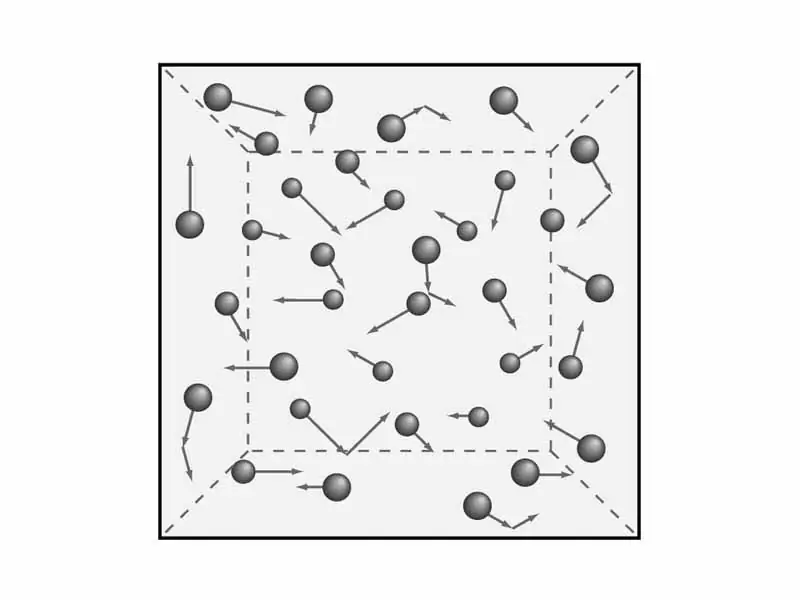
Kuna haja ya kuelewa masharti ya nadharia ya gesi. Kama tulivyosema hapo awali, tutazingatia sifa za jumla za gesi, kama vile shinikizo na joto. Hii niitahitajika baadaye ili kupata mlingano wa nadharia ya molekiuli-kinetiki ya gesi. Lakini hisabati - baadaye, na sasa tushughulike na nadharia na, ipasavyo, fizikia.
Wanasayansi wameunda vipengele vitano vya nadharia ya molekuli ya gesi, ambayo hutumika kufahamu muundo wa kinetiki wa gesi. Zinasikika hivi:
- Gesi zote zinaundwa na chembe za msingi ambazo hazina saizi fulani, lakini zina uzito fulani. Kwa maneno mengine, ujazo wa chembe hizi ni mdogo ikilinganishwa na urefu kati yao.
- Atomi na molekuli za gesi kwa kweli hazina nishati inayoweza kutokea, mtawalia, kwa mujibu wa sheria, nishati yote ni sawa na kinetiki.
- Tayari tulifahamiana na nafasi hii mapema - Mwendo wa Brownian. Hiyo ni, chembe za gesi huwa katika mwendo wa kuendelea na wa mtafaruku.
- Hakika migongano yote ya kuheshimiana ya chembe za gesi, ikiambatana na ujumbe wa kasi na nishati, ni laini kabisa. Hii ina maana kwamba hakuna hasara ya nishati au kuruka kwa kasi katika nishati yao ya kinetiki wakati wa mgongano.
- Katika hali ya kawaida na halijoto isiyobadilika, wastani wa nishati ya mwendo wa chembe za gesi zote ni sawa.
Tunaweza kuandika upya nafasi ya tano kupitia aina hii ya mlingano wa nadharia ya kimolekuli-kinetiki ya gesi:
E=1/2mv^2=3/2kT, ambapo k ni kiashiria kisichobadilika cha Boltzmann; T - halijoto katika Kelvin.
Mlinganyo huu hutufanya kuelewa uhusiano kati ya kasi ya chembe msingi za gesi na halijoto yake kamili. Ipasavyo, juu kabisa yaohalijoto, ndivyo kasi yao na nishati ya kinetic inavyoongezeka.
Shinikizo la gesi
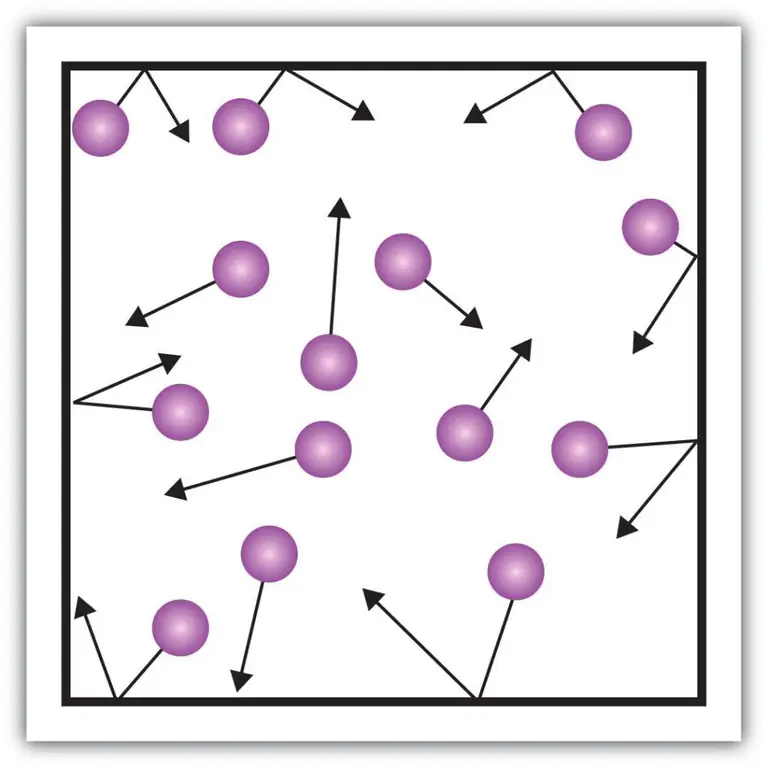
Vipengele vikubwa vya sifa kama hivyo, kama vile shinikizo la gesi, vinaweza pia kuelezwa kwa kutumia nadharia ya kinetiki. Ili kufanya hivyo, hebu tufikirie mfano ufuatao.
Hebu tuchukulie kwamba molekuli ya baadhi ya gesi iko kwenye sanduku, ambayo urefu wake ni L. Hebu tutumie vifungu vya nadharia ya gesi iliyoelezwa hapo juu na kuzingatia ukweli kwamba tufe ya molekuli inasonga tu kando ya x. -mhimili. Kwa hivyo, tutaweza kuchunguza mchakato wa mgongano wa elastic na moja ya kuta za chombo (sanduku).
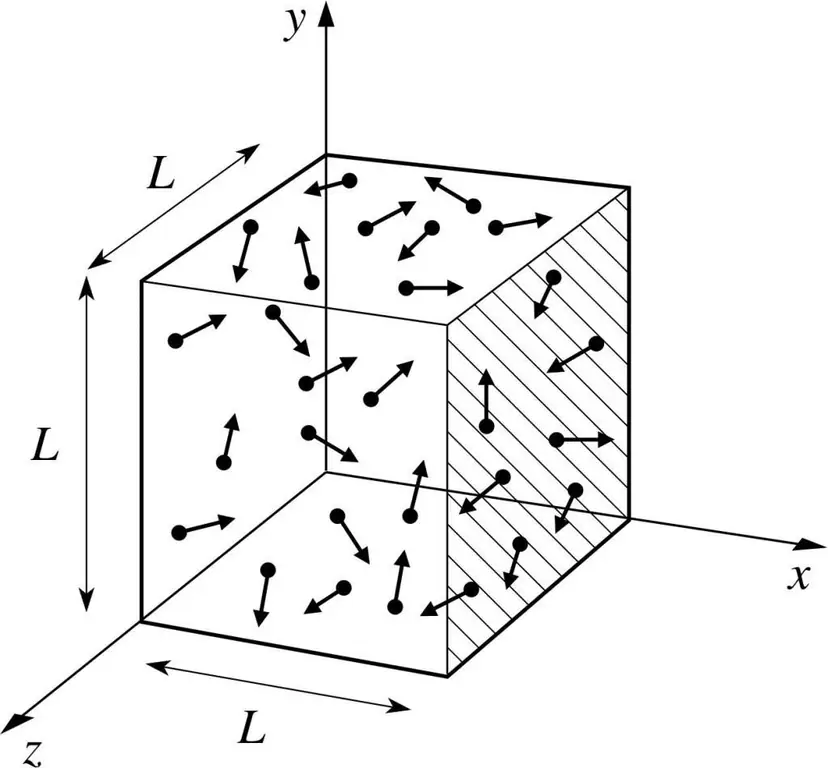
Msisitizo wa mgongano unaoendelea, kama tujuavyo, unabainishwa na fomula: p=mv, lakini katika hali hii, fomula hii itachukua fomu ya makadirio: p=mv(x).
Kwa kuwa tunazingatia tu mwelekeo wa mhimili wa x, yaani, mhimili wa x, badiliko la jumla la mwendo litaonyeshwa na fomula: mv(x) - m(-v(x))=2mv(x).
Inayofuata, zingatia nguvu inayotekelezwa na kifaa chetu kwa kutumia sheria ya pili ya Newton: F=ma=P/t.
Kutoka kwa fomula hizi tunaonyesha shinikizo kutoka upande wa gesi: P=F/a;
Sasa hebu tubadilishe usemi wa nguvu katika fomula inayotokana na tupate: P=mv(x)^2/L^3.
Baada ya hapo, fomula yetu iliyokamilishwa ya shinikizo inaweza kuandikwa kwa nambari ya N-th ya molekuli za gesi. Kwa maneno mengine, itaonekana kama hii:
P=Nmv(x)^2/V, ambapo v ni kasi na V ni sauti.
Sasa hebu tujaribu kuangazia masharti machache ya msingi kuhusu shinikizo la gesi:
- Inajidhihirisha kupitiamigongano ya molekuli na molekuli za kuta za kitu ambamo kimo.
- Ukubwa wa shinikizo ni sawia moja kwa moja na nguvu na kasi ya athari ya molekuli kwenye kuta za chombo.
Hitimisho fupi kuhusu nadharia
Kabla hatujaenda mbele zaidi na kuzingatia mlingano wa kimsingi wa nadharia ya kinetiki ya molekuli, tunakupa hitimisho fupi kutoka kwa hoja na nadharia iliyo hapo juu:
- Kipimo cha wastani wa nishati ya mwendo wa atomi na molekuli zake ni halijoto kamili.
- Gesi mbili tofauti zinapokuwa kwenye halijoto sawa, molekuli zake huwa na wastani wa nishati ya kinetiki sawa.
- Nishati ya chembe za gesi inalingana moja kwa moja na wastani wa kasi ya mraba: E=1/2mv^2.
- Ingawa molekuli za gesi zina wastani wa nishati ya kinetiki, mtawalia, na kasi ya wastani, chembe mahususi husogea kwa kasi tofauti: nyingine haraka, nyingine polepole.
- Kadiri halijoto inavyoongezeka, ndivyo kasi ya molekuli inavyoongezeka.
- Ni mara ngapi tunaongeza joto la gesi (kwa mfano, maradufu), nishati ya mwendo wa chembe zake huongezeka mara nyingi (mtawalia, maradufu).
Mlingano wa kimsingi na fomula

Mlinganyo wa kimsingi wa nadharia ya kinetiki ya molekuli hukuruhusu kuanzisha uhusiano kati ya idadi ya ulimwengu mdogo na, ipasavyo, makroskopu, yaani, kipimo, kiasi.
Mojawapo ya miundo rahisi zaidi ambayo nadharia ya molekuli inaweza kuzingatia ni muundo bora wa gesi.
Unaweza kusema hivyohii ni aina ya modeli ya kufikirika iliyochunguzwa na nadharia ya kinetiki ya molekuli ya gesi bora, ambamo:
- chembe rahisi zaidi za gesi huchukuliwa kuwa mipira inayonyumbulika kabisa ambayo huingiliana na kila mmoja na kwa molekuli za kuta za chombo chochote katika hali moja tu - mgongano wa elastic kabisa;
- nguvu za mvuto ndani ya gesi hazipo, au zinaweza kupuuzwa;
- vipengele vya muundo wa ndani wa gesi vinaweza kuchukuliwa kama nyenzo, yaani, kiasi chao pia kinaweza kupuuzwa.
Kwa kuzingatia mwanamitindo kama huyo, mwanafizikia mzaliwa wa Ujerumani Rudolf Clausius aliandika fomula ya shinikizo la gesi kupitia uhusiano wa vigezo vidogo na vikubwa. Inaonekana kama:
p=1/3m(0)nv^2.
Baadaye fomula hii itaitwa mlingano wa kimsingi wa nadharia ya kimolekuli-kinetiki ya gesi bora. Inaweza kuwasilishwa kwa fomu kadhaa tofauti. Jukumu letu sasa ni kuonyesha sehemu kama vile fizikia ya molekuli, nadharia ya kinetiki ya molekuli, na kwa hivyo milinganyo na aina zao kamili. Kwa hivyo, inaleta maana kuzingatia tofauti zingine za fomula ya kimsingi.
Tunajua kwamba wastani wa nishati inayoashiria mwendo wa molekuli za gesi inaweza kupatikana kwa kutumia fomula: E=m(0)v^2/2.
Katika hali hii, tunaweza kubadilisha usemi m(0)v^2 katika fomula asili ya shinikizo kwa wastani wa nishati ya kinetiki. Kutokana na hili, tutakuwa na fursa ya kutunga equation ya msingi ya nadharia ya kinetic ya molekuli ya gesi katika fomu ifuatayo: p=2/3nE.
Mbali na hilo, sote tunajua kwamba usemi m(0)n unaweza kuandikwa kama zao la nukuu mbili:
m/NN/V=m/V=ρ.
Baada ya upotoshaji huu, tunaweza kuandika upya fomula yetu ya mlingano wa nadharia ya molekuli-kinetiki ya gesi bora katika umbo la tatu, tofauti:
p=1/3ρv^2.
Vema, labda hayo ndiyo tu unahitaji kujua kuhusu mada hii. Inabakia tu kupanga maarifa yaliyopatikana kwa njia ya hitimisho fupi (na si hivyo).
Hitimisho zote za jumla na fomula kuhusu mada "Nadharia ya Molecular-kinetic"
Kwa hivyo tuanze.
Kwanza:
Fizikia ni sayansi ya kimsingi iliyojumuishwa katika kozi ya sayansi asilia, ambayo huchunguza sifa za mata na nishati, muundo wao, mifumo ya asili isokaboni.
Inajumuisha sehemu zifuatazo:
- mekaniki (kinematiki na mienendo);
- tuli;
- thermodynamics;
- electrodynamics;
- sehemu ya molekuli;
- optics;
- fizikia ya quantumu na kiini cha atomiki.
Pili:
Fizikia ya chembe na thermodynamics ni matawi yanayohusiana kwa karibu ambayo huchunguza sehemu ya kipekee ya idadi ya mifumo halisi, yaani, mifumo inayojumuisha idadi kubwa ya chembe msingi.
Zinatokana na nadharia ya kinetiki ya molekuli.
Tatu:
Kiini cha mambo ni hiki. Nadharia ya kinetiki ya molekuli inaelezea kwa undani muundo wa dutu (mara nyingi muundo wa gesi kuliko yabisi).na miili ya kioevu), kwa kuzingatia mawazo matatu ya kimsingi ambayo yalikusanywa kutoka kwa mawazo ya wanasayansi mashuhuri. Miongoni mwao: Robert Hooke, Isaac Newton, Daniel Bernoulli, Mikhail Lomonosov na wengine wengi.
Nne:
Nyengo tatu za msingi za nadharia ya kinetiki ya molekuli:
- Dutu zote (bila kujali ni kioevu, kigumu au gesi) zina muundo changamano unaojumuisha chembe ndogo zaidi: molekuli na atomi.
- Chembechembe hizi zote rahisi ziko katika mwendo wa mtafaruku unaoendelea. Mfano: Mwendo wa rangi ya hudhurungi na mtawanyiko.
- Molekuli zote chini ya hali yoyote huingiliana kwa nguvu fulani ambazo zina miamba ya umeme.
Kila moja ya masharti haya ya nadharia ya kinetiki ya molekuli ni msingi thabiti katika uchunguzi wa muundo wa maada.
Ya tano:
Njia kuu kadhaa za nadharia ya molekiuli ya muundo wa gesi:
- Gesi zote zinaundwa na chembe za msingi ambazo hazina saizi fulani, lakini zina uzito fulani. Kwa maneno mengine, ujazo wa chembe hizi ni mdogo ikilinganishwa na umbali kati yao.
- Atomi na molekuli za gesi kwa kweli hazina nishati inayoweza kutokea, mtawalia, nishati yake yote ni sawa na ile ya kinetiki.
- Tayari tulifahamiana na nafasi hii mapema - Mwendo wa Brownian. Hiyo ni, chembe za gesi huwa katika mwendo wa kuendelea na nasibu.
- Kwa hakika migongano yote ya pande zote ya atomi na molekuli za gesi, ikiambatana na ujumbe wa kasi na nishati, ni nyororo kabisa. Hii niinamaanisha kuwa hakuna hasara ya nishati au kuruka kwa kasi katika nishati yao ya kinetiki wakati wa mgongano.
- Katika hali ya kawaida na halijoto isiyobadilika, wastani wa nishati ya kinetiki ya takriban gesi zote ni sawa.
Ya sita:
Hitimisho kutoka kwa nadharia ya gesi:
- Joto kamili ni kipimo cha wastani wa nishati ya kinetiki ya atomi na molekuli zake.
- Gesi mbili tofauti zinapokuwa kwenye halijoto sawa, molekuli zake huwa na wastani wa nishati ya kinetiki sawa.
- Wastani wa nishati ya kinetiki ya chembe za gesi inalingana moja kwa moja na mzizi wa kasi ya mraba: E=1/2mv^2.
- Ingawa molekuli za gesi zina wastani wa nishati ya kinetiki, mtawalia, na kasi ya wastani, chembe mahususi husogea kwa kasi tofauti: nyingine haraka, nyingine polepole.
- Kadiri halijoto inavyoongezeka, ndivyo kasi ya molekuli inavyoongezeka.
- Ni mara ngapi tunaongeza joto la gesi (kwa mfano, maradufu), wastani wa nishati ya kinetiki ya chembe zake pia huongezeka mara nyingi sana (mtawalia, maradufu).
- Uhusiano kati ya shinikizo la gesi kwenye kuta za chombo ambamo iko na ukubwa wa athari za molekuli kwenye kuta hizi ni sawia moja kwa moja: kadiri athari zinavyoongezeka, ndivyo shinikizo inavyoongezeka, na kinyume chake..
Ya saba:
Muundo bora wa gesi ni modeli ambayo masharti yafuatayo lazima yatimizwe:
- Molekuli za gesi zinaweza na kuzingatiwa kama mipira nyororo.
- Mipira hii inaweza kuingiliana na kuta za yoyotechombo katika hali moja tu - mgongano elastic kabisa.
- Nguvu hizo zinazoelezea msukumo kati ya atomi na molekuli za gesi hazipo au zinaweza kupuuzwa.
- Atomu na molekuli huzingatiwa kama pointi za nyenzo, yaani, ujazo wao pia unaweza kupuuzwa.
Ya nane:
Hebu tupe milinganyo yote ya kimsingi na tuonyeshe fomula katika mada "Nadharia ya Molekuli-kinetiki":
p=1/3m(0)nv^2 - mlinganyo msingi wa muundo bora wa gesi, unaotolewa na mwanafizikia Mjerumani Rudolf Clausius.
p=2/3nE - mlingano wa kimsingi wa nadharia ya kimolekuli-kinetiki ya gesi bora. Inatokana na wastani wa nishati ya kinetiki ya molekuli.
р=1/3ρv^2 - mlinganyo sawa, lakini unaozingatiwa kupitia msongamano na mzizi wa kasi ya mraba ya molekuli bora za gesi.
m(0)=M/N(a) - fomula ya kutafuta wingi wa molekuli moja kupitia nambari ya Avogadro.
v^2=(v(1)+v(2)+v(3)+…)/N - fomula ya kutafuta wastani wa kasi ya mraba ya molekuli, ambapo v(1), v(2), v (3) na kadhalika - kasi ya molekuli ya kwanza, ya pili, ya tatu na kadhalika hadi molekuli ya nth.
n=N/V - fomula ya kutafuta mkusanyiko wa molekuli, ambapo N ni idadi ya molekuli katika ujazo wa gesi hadi ujazo fulani V.
E=mv^2/2=3/2kT - fomula za kutafuta wastani wa nishati ya kinetiki ya molekuli, ambapo v^2 ndio mzizi wa kasi ya mraba ya molekuli, k thamani iliyopewa jina la Mwaustria fizikia ya Ludwig Boltzmann, na T ni halijoto ya gesi.
p=nkT - fomula ya shinikizo katika suala la mkusanyiko, thabitiBoltzmann na halijoto kamili T. Kutoka humo hufuata kanuni nyingine ya msingi, iliyogunduliwa na mwanasayansi wa Kirusi Mendeleev na mwanafizikia-mhandisi wa Kifaransa Claiperon:
pV=m/MRT, ambapo R=kN(a) ni hali thabiti ya ulimwengu kwa gesi.
Sasa hebu tuonyeshe viunga kwa michakato tofauti ya iso: isobariki, isochoric, isothermal na adiabatic.
pV/T=const - hutekelezwa wakati wingi na muundo wa gesi ni thabiti.
рV=consst - ikiwa halijoto pia ni thabiti.
V/T=consst - ikiwa shinikizo la gesi ni thabiti.
p/T=consst - ikiwa sauti ni thabiti.
Labda hivyo ndivyo tu unahitaji kujua kuhusu mada hii.
Leo tumejikita katika nyanja ya kisayansi kama vile fizikia ya nadharia, sehemu zake nyingi na vizuizi. Kwa undani zaidi, tuligusia eneo la fizikia kama fizikia ya kimsingi ya Masi na thermodynamics, ambayo ni, nadharia ya Masi-kinetic, ambayo, inaonekana, haitoi shida yoyote katika utafiti wa awali, lakini kwa kweli ina mitego mingi.. Inapanua uelewa wetu wa mfano bora wa gesi, ambao pia tulijifunza kwa undani. Kwa kuongezea, inafaa kuzingatia kwamba pia tulifahamiana na hesabu za kimsingi za nadharia ya Masi katika tofauti zao tofauti, na pia tukazingatia kanuni zote muhimu zaidi za kupata idadi fulani isiyojulikana juu ya mada hii. Hii itakuwa muhimu sana wakati wa kuandaa kuandika. majaribio yoyote, mitihani na majaribio, au kupanua mtazamo wa jumla na ujuzi wa fizikia.
Tunatumai kwamba makala haya yalikuwa na manufaa kwako, na umetoa habari muhimu tu kutoka kwayo, ukiimarisha ujuzi wako katika nguzo kama vile thermodynamics kama masharti ya msingi ya nadharia ya kinetiki ya molekuli.






