Sehemu muhimu ya thermodynamics ni uchunguzi wa mabadiliko kati ya awamu tofauti za dutu, kwa kuwa michakato hii hutokea kwa vitendo na ni ya umuhimu wa kimsingi kwa kutabiri tabia ya mfumo chini ya hali fulani. Mabadiliko haya yanaitwa mabadiliko ya awamu, ambayo makala yametolewa.
Dhana ya awamu na kijenzi cha mfumo

Kabla ya kuendelea na uzingatiaji wa mabadiliko ya awamu katika fizikia, ni muhimu kufafanua dhana ya awamu yenyewe. Kama inavyojulikana kutoka kwa mwendo wa fizikia ya jumla, kuna hali tatu za suala: gesi, dhabiti na kioevu. Katika sehemu maalum ya sayansi - katika thermodynamics - sheria zinaundwa kwa awamu za suala, na sio kwa majimbo yao ya mkusanyiko. Awamu inaeleweka kama ujazo fulani wa maada ambao una muundo wa homogeneous, unaojulikana kwa sifa mahususi za kimwili na kemikali na hutenganishwa na maada nyingine kwa mipaka, ambayo huitwa interphase.
Kwa hivyo, dhana ya "awamu" hubeba taarifa muhimu zaidi kuhusu sifa.jambo kuliko hali yake ya kujumlisha. Kwa mfano, hali dhabiti ya chuma kama vile chuma inaweza kuwa katika awamu zifuatazo: ujazo wa kitovu cha sumaku ya joto la chini (BCC), bcc isiyo na sumaku ya halijoto ya chini, ujazo unaozingatia uso (fcc), na juu- halijoto isiyo ya sumaku bcc.
Mbali na dhana ya "awamu", sheria za thermodynamics pia hutumia neno "vipengele", ambalo linamaanisha idadi ya vipengele vya kemikali vinavyounda mfumo fulani. Hii inamaanisha kuwa awamu inaweza kuwa sehemu moja (kipengele 1 cha kemikali) au sehemu nyingi (vipengele kadhaa vya kemikali).
nadharia ya Gibbs na usawa kati ya awamu za mfumo

Ili kuelewa mabadiliko ya awamu, ni muhimu kujua hali ya usawa kati yao. Masharti haya yanaweza kupatikana kihisabati kwa kutatua mfumo wa milinganyo ya Gibbs kwa kila mojawapo, ikizingatiwa kuwa hali ya msawazo inafikiwa wakati jumla ya nishati ya Gibbs ya mfumo iliyotengwa na ushawishi wa nje inakoma kubadilika.
Kutokana na kusuluhisha mfumo ulioonyeshwa wa milinganyo, hali hupatikana kwa kuwepo kwa usawa kati ya awamu kadhaa: mfumo uliotengwa utakoma kubadilika tu wakati shinikizo, uwezo wa kemikali wa kila sehemu na halijoto katika awamu zote. ni sawa kwa kila mmoja.
Sheria ya awamu ya Gibbs ya usawa

Mfumo unaojumuisha awamu na vijenzi kadhaa unaweza kuwa katika usawa si tuchini ya hali fulani, kwa mfano, kwa joto maalum na shinikizo. Baadhi ya vigeu katika nadharia ya Gibbs kwa usawa vinaweza kubadilishwa wakati wa kudumisha idadi ya awamu na idadi ya vijenzi vilivyo katika msawazo huu. Idadi ya vigeu vinavyoweza kubadilishwa bila kusumbua usawa katika mfumo inaitwa idadi ya uhuru wa mfumo huu.
Idadi ya uhuru l wa mfumo unaojumuisha awamu f na vijenzi vya k hubainishwa kipekee kutoka kwa kanuni ya awamu ya Gibbs. Sheria hii imeandikwa kwa hisabati kama ifuatavyo: l + f=k + 2. Jinsi ya kufanya kazi na sheria hii? Rahisi sana. Kwa mfano, inajulikana kuwa mfumo una f=3 awamu za usawa. Ni idadi gani ya chini ya vifaa ambavyo mfumo kama huo unaweza kuwa na? Unaweza kujibu swali kwa hoja kama ifuatavyo: katika kesi ya usawa, hali ngumu zaidi zipo wakati inagunduliwa tu kwa viashiria fulani, ambayo ni, mabadiliko katika paramu yoyote ya thermodynamic itasababisha usawa. Hii ina maana kwamba idadi ya uhuru l=0. Kubadilisha maadili yanayojulikana ya l na f, tunapata k=1, yaani, mfumo ambao awamu tatu ziko katika usawa unaweza kujumuisha sehemu moja. Mfano mkuu ni sehemu tatu za maji, ambapo barafu, maji kimiminika na mvuke huwepo kwa usawa katika halijoto na shinikizo mahususi.
Uainishaji wa mabadiliko ya awamu
Ukianza kubadilisha baadhi ya vigezo vya halijoto katika mfumo ulio katika usawa, unaweza kuona jinsi awamu moja itatoweka na nyingine kuonekana. Mfano rahisi wa mchakato huu ni kuyeyuka kwa barafu wakati inapokanzwa.
Ikizingatiwa kuwa mlinganyo wa Gibbs unategemea tu vigeu viwili (shinikizo na halijoto), na mpito wa awamu unahusisha mabadiliko katika vigeu hivi, basi kimahesabu mpito kati ya awamu unaweza kuelezewa kwa kutofautisha nishati ya Gibbs kwa heshima yake. vigezo. Ilikuwa ni mbinu hii ambayo ilitumiwa na mwanafizikia wa Austria Paul Ehrenfest mwaka wa 1933, alipokusanya uainishaji wa michakato yote inayojulikana ya thermodynamic ambayo hutokea kwa mabadiliko katika usawa wa awamu.
Kutokana na misingi ya thermodynamics, inafuata kwamba kitomio cha kwanza cha nishati ya Gibbs kuhusiana na halijoto ni sawa na mabadiliko katika entropi ya mfumo. Derivative ya nishati ya Gibbs kwa heshima na shinikizo ni sawa na mabadiliko ya kiasi. Ikiwa, wakati awamu katika mfumo zinabadilika, entropy au sauti inakabiliwa na mapumziko, yaani, hubadilika ghafla, basi wanazungumza juu ya mpito wa awamu ya kwanza.
Zaidi ya hayo, viini vya pili vya nishati ya Gibbs kuhusiana na halijoto na shinikizo ni uwezo wa joto na mgawo wa upanuzi wa ujazo, mtawalia. Ikiwa mabadiliko kati ya awamu yanafuatana na kutoendelea kwa maadili ya kiasi cha kimwili kilichoonyeshwa, basi mtu anazungumzia mpito wa awamu ya pili.
Mifano ya mabadiliko kati ya awamu

Kuna idadi kubwa ya mabadiliko tofauti katika asili. Ndani ya mfumo wa uainishaji huu, mifano ya kuvutia ya mabadiliko ya aina ya kwanza ni michakato ya kuyeyuka kwa metali au kufidia kwa mvuke wa maji kutoka kwa hewa, wakati kuna kuruka kwa sauti kwenye mfumo.
Iwapo tunazungumza kuhusu mabadiliko ya mpangilio wa pili, basi mifano ya kuvutia ni mabadiliko ya chuma kutoka hali ya sumaku hadi paramagnetic katika halijoto.768 ºC au ugeuzaji wa kondakta wa metali kuwa hali ya upitishaji maji katika halijoto iliyo karibu na sufuri kabisa.
Milingano inayoelezea mabadiliko ya aina ya kwanza
Katika mazoezi, mara nyingi ni muhimu kujua jinsi halijoto, shinikizo na nishati iliyonyonywa (iliyotolewa) inavyobadilika katika mfumo wakati mabadiliko ya awamu yanatokea ndani yake. Equations mbili muhimu hutumiwa kwa kusudi hili. Zinapatikana kwa kuzingatia ujuzi wa misingi ya thermodynamics:
- Mchanganyiko wa Clapeyron, ambao huanzisha uhusiano kati ya shinikizo na halijoto wakati wa mabadiliko kati ya awamu tofauti.
- Fomula ya Clausius inayounganisha nishati iliyonyonywa (iliyotolewa) na halijoto ya mfumo wakati wa mageuzi.
Matumizi ya milinganyo yote miwili si tu katika kupata utegemezi wa kiasi cha kiasi halisi, lakini pia katika kubainisha ishara ya mteremko wa mikondo ya msawazo kwenye michoro ya awamu.
Mlinganyo wa kuelezea mabadiliko ya aina ya pili

Mabadiliko ya awamu ya aina ya 1 na 2 yanafafanuliwa kwa milinganyo tofauti, kwa kuwa matumizi ya milinganyo ya Clausius na Clausius kwa mabadiliko ya mpangilio wa pili husababisha kutokuwa na uhakika wa kihisabati.
Ili kuelezea mwisho, milinganyo ya Ehrenfest hutumiwa, ambayo huanzisha uhusiano kati ya mabadiliko ya shinikizo na halijoto kupitia ujuzi wa mabadiliko ya uwezo wa joto na mgawo wa upanuzi wa ujazo wakati wa mchakato wa kubadilisha. Milinganyo ya Ehrenfest inatumika kuelezea mipito ya kondakta-superconductor bila uga wa sumaku.
Umuhimumichoro ya awamu
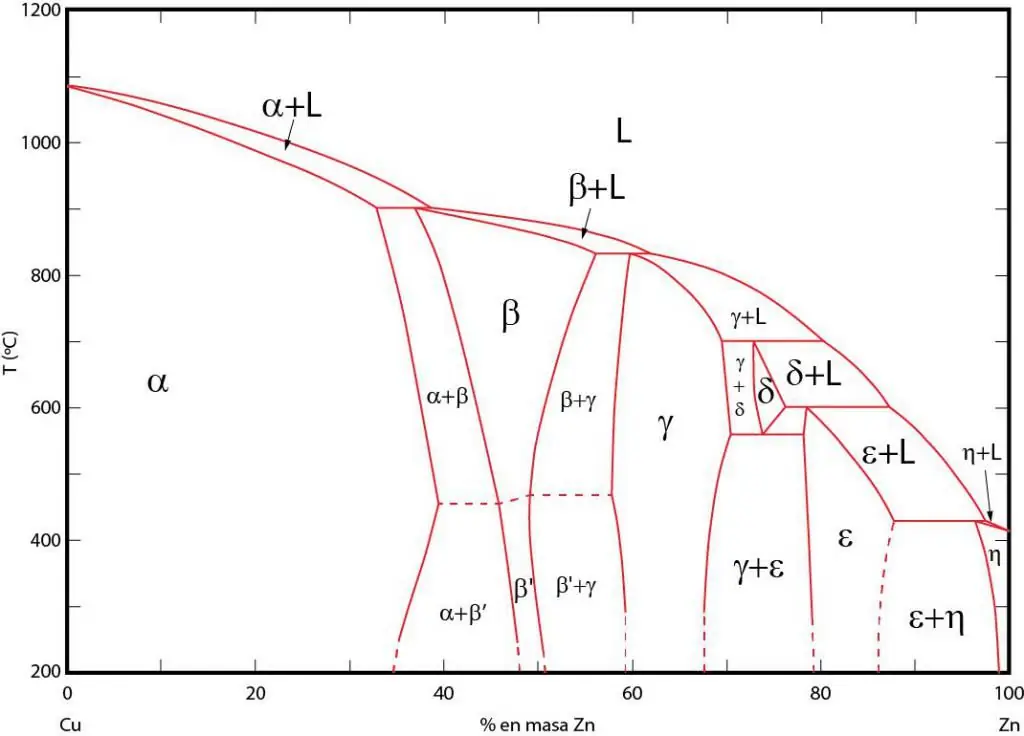
Michoro ya Awamu ni uwakilishi wa picha wa maeneo ambayo awamu zinazolingana zipo katika usawa. Maeneo haya yanatenganishwa na mistari ya usawa kati ya awamu. P-T (joto-shinikizo), T-V (joto-kiasi), na michoro ya awamu ya P-V (shinikizo-kiasi) hutumiwa mara nyingi.
Umuhimu wa michoro ya awamu upo katika ukweli kwamba inakuwezesha kutabiri mfumo utakuwa katika awamu gani hali ya nje inapobadilika ipasavyo. Taarifa hii hutumiwa katika matibabu ya joto ya nyenzo mbalimbali ili kupata muundo na sifa zinazohitajika.






