Thermodynamics ni tawi muhimu la fizikia. Tunaweza kusema kwa usalama kwamba mafanikio yake yamesababisha kuibuka kwa enzi ya kiteknolojia na kwa kiasi kikubwa kuamua mwendo wa historia ya mwanadamu katika miaka 300 iliyopita. Kifungu kinajadili sheria ya kwanza, ya pili na ya tatu ya thermodynamics na matumizi yake katika mazoezi.
Thermodynamics ni nini?
Kabla ya kutunga sheria za thermodynamics, hebu tubaini ni nini sehemu hii ya fizikia inafanya.
Neno "thermodynamics" lina asili ya Kigiriki na linamaanisha "mwendo kutokana na joto". Hiyo ni, tawi hili la fizikia linajishughulisha na utafiti wa michakato yoyote, kama matokeo ambayo nishati ya joto inabadilishwa kuwa mwendo wa mitambo na kinyume chake.
Sheria za kimsingi za thermodynamics ziliundwa katikati ya karne ya 19. Sayansi ya "harakati na joto" inazingatia tabia ya mfumo mzima kwa ujumla, kusoma mabadiliko katika vigezo vyake vya macroscopic - joto, shinikizo na kiasi, na si kulipa kipaumbele kwa muundo wake wa microscopic. Aidha, wa kwanza wao ana jukumu la msingi katika uundaji wa sheriathermodynamics katika fizikia. Inashangaza kutambua kwamba yametokana tu na uchunguzi wa majaribio.
Dhana ya mfumo wa thermodynamic

Inamaanisha kundi lolote la atomi, molekuli au vipengele vingine vinavyozingatiwa kwa ujumla wake. Sheria zote tatu zimeundwa kwa kinachojulikana mfumo wa thermodynamic. Mifano ni: angahewa ya dunia, kiumbe hai chochote, mchanganyiko wa gesi kwenye injini ya mwako ndani, n.k.
Mifumo yote katika thermodynamics ni ya mojawapo ya aina tatu:
- Fungua. Wanabadilishana joto na suala na mazingira. Kwa mfano, ikiwa chakula hupikwa kwenye sufuria kwenye moto wazi, basi hii ni mfano wazi wa mfumo wazi, kwani sufuria hupokea nishati kutoka kwa mazingira ya nje (moto), wakati yenyewe huangaza nishati kwa namna ya joto. na maji pia huvukiza kutoka humo (metabolism)
- Imefungwa. Katika mifumo kama hiyo hakuna kubadilishana vitu na mazingira, ingawa ubadilishaji wa nishati hufanyika. Kurudi kwenye kesi ya awali: ikiwa unafunika kettle na kifuniko, unaweza kupata mfumo uliofungwa.
- Kutengwa. Hii ni aina ya mifumo ya thermodynamic ambayo haibadilishi maada au nishati na nafasi inayozunguka. Mfano unaweza kuwa thermos iliyo na chai ya moto.
Kiwango cha joto

Dhana hii inamaanisha nishati ya kinetic ya chembe zinazounda miili inayozunguka, ambayo huakisi kasi.mwendo wa nasibu wa chembe. Kubwa ni, joto la juu. Ipasavyo, kwa kupunguza nishati ya kinetiki ya mfumo, tunaipoza.
Dhana hii ina maana ya nishati ya kinetiki ya chembe zinazounda miili inayozunguka, ambayo huakisi kasi ya mwendo wa fujo wa chembe. Kubwa ni, joto la juu. Ipasavyo, kwa kupunguza nishati ya kinetiki ya mfumo, tunaipoza.
Joto la joto huonyeshwa katika SI (Mfumo wa Kimataifa wa Vitengo) huko Kelvin (kwa heshima ya mwanasayansi wa Uingereza William Kelvin, ambaye alipendekeza kipimo hiki kwanza). Kuelewa sheria ya kwanza, ya pili na ya tatu ya thermodynamics haiwezekani bila ufafanuzi wa hali ya joto.
Mgawanyiko wa digrii moja kwenye mizani ya Kelvin pia inalingana na digrii moja ya Selsiasi. Ubadilishaji kati ya vitengo hivi unafanywa kulingana na fomula: TK =TC + 273, 15, ambapo TK na TC - halijoto katika kelvins na nyuzi joto Selsiasi mtawalia.
Upekee wa mizani ya Kelvin ni kwamba haina maadili hasi. Sifuri ndani yake (TC=-273, 15 oC) inalingana na hali wakati mwendo wa joto wa chembe za mfumo haupo kabisa., zinaonekana kuwa "zimeganda".
Uhifadhi wa nishati na sheria ya 1 ya thermodynamics

Mnamo 1824, Nicolas Léonard Sadi Carnot, mhandisi na mwanafizikia Mfaransa, alitoa pendekezo la ujasiri ambalo sio tu liliongoza kwa maendeleo ya fizikia, lakini pia likawa hatua kuu katika uboreshaji wa teknolojia. Yakeinaweza kutengenezwa kama ifuatavyo: "Nishati haiwezi kuundwa au kuharibiwa, inaweza tu kuhamishwa kutoka jimbo moja hadi jingine."
Kwa kweli, maneno ya Sadi Carnot yanasisitiza sheria ya uhifadhi wa nishati, ambayo iliunda msingi wa sheria ya 1 ya thermodynamics: "Kila wakati mfumo unapokea nishati kutoka nje, huibadilisha kuwa aina nyingine, kuu ya ambazo ni za joto na za mitambo."
Mfumo wa hisabati wa sheria ya 1 imeandikwa kama ifuatavyo:
Q=ΔU + A, hapa Q ni kiasi cha joto kinachohamishwa na mazingira hadi kwenye mfumo, ΔU ni badiliko la nishati ya ndani ya mfumo huu, A ni kazi kamili ya mitambo.
Michakato ya Adiabatic
Mfano wao mzuri ni harakati za hewa kwenye miteremko ya milima. Misa kama hiyo ni kubwa (kilomita au zaidi), na hewa ni insulator bora ya joto. Sifa zilizobainishwa huturuhusu kuzingatia michakato yoyote na misa ya hewa inayotokea ndani ya muda mfupi kama adiabatic. Wakati hewa inapoinuka kwenye mteremko wa mlima, shinikizo lake hupungua, huongezeka, yaani, hufanya kazi ya mitambo, na, kwa sababu hiyo, hupungua. Kinyume chake, harakati ya chini ya molekuli ya hewa inaambatana na ongezeko la shinikizo ndani yake, inapunguza na, kutokana na hili, inakuwa moto sana.
Utumiaji wa sheria ya thermodynamics, ambayo ilijadiliwa katika kichwa kidogo kilichopita, inaonyeshwa kwa urahisi zaidi kwa kutumia mfano wa mchakato wa adiabatic.
Kulingana na ufafanuzi, kama matokeo yake hakuna kubadilishana nishati namazingira, yaani, katika equation hapo juu, Q=0. Hii inaongoza kwa usemi ufuatao: ΔU=-A. Ishara ya minus hapa ina maana kwamba mfumo hufanya kazi ya mitambo kwa kupunguza nishati yake ya ndani. Ikumbukwe kwamba nishati ya ndani inategemea moja kwa moja halijoto ya mfumo.
mwelekeo wa michakato ya joto
Suala hili linahusu sheria ya 2 ya thermodynamics. Hakika kila mtu aliona kwamba ikiwa unaleta vitu viwili vilivyo na joto tofauti katika kuwasiliana, basi baridi itawaka kila wakati, na ya moto itapungua. Kumbuka kwamba mchakato wa kurudi nyuma unaweza kutokea ndani ya mfumo wa sheria ya kwanza ya thermodynamics, lakini hautekelezwi kamwe kwa vitendo.
Sababu ya kutoweza kutenduliwa kwa mchakato huu (na michakato yote inayojulikana Ulimwenguni) ni mpito wa mfumo hadi katika hali inayowezekana zaidi. Katika mfano unaozingatiwa na mguso wa miili miwili ya halijoto tofauti, hali inayowezekana zaidi itakuwa ile ambayo chembe zote za mfumo zitakuwa na nishati sawa ya kinetiki.
Sheria ya pili ya thermodynamics inaweza kutengenezwa kama ifuatavyo: "Joto haliwezi kamwe kuhamishwa moja kwa moja kutoka kwa mwili baridi hadi kwenye moto." Ikiwa tutaanzisha dhana ya entropy kama kipimo cha shida, basi inaweza kuwakilishwa kama ifuatavyo: "Mchakato wowote wa thermodynamic huendelea na ongezeko la entropy".
Injini ya joto

Neno hili linaeleweka kama mfumo ambao, kutokana na usambazaji wa nishati ya nje kwake, unaweza kufanya kazi ya kiufundi. Kwanzainjini za joto zilikuwa injini za mvuke na zilivumbuliwa mwishoni mwa karne ya 17.
Sheria ya pili ya thermodynamics ina jukumu muhimu katika kubainisha ufanisi wao. Sadi Carnot pia aligundua kuwa ufanisi wa juu wa kifaa hiki ni: Ufanisi=(T2 - T1)/T2, hapa T2 na T1 ni hita na halijoto ya friji. Kazi ya mitambo inaweza tu kufanywa wakati kuna mtiririko wa joto kutoka kwa mwili moto hadi kwenye baridi, na mtiririko huu hauwezi kubadilishwa kwa 100% kuwa nishati muhimu.
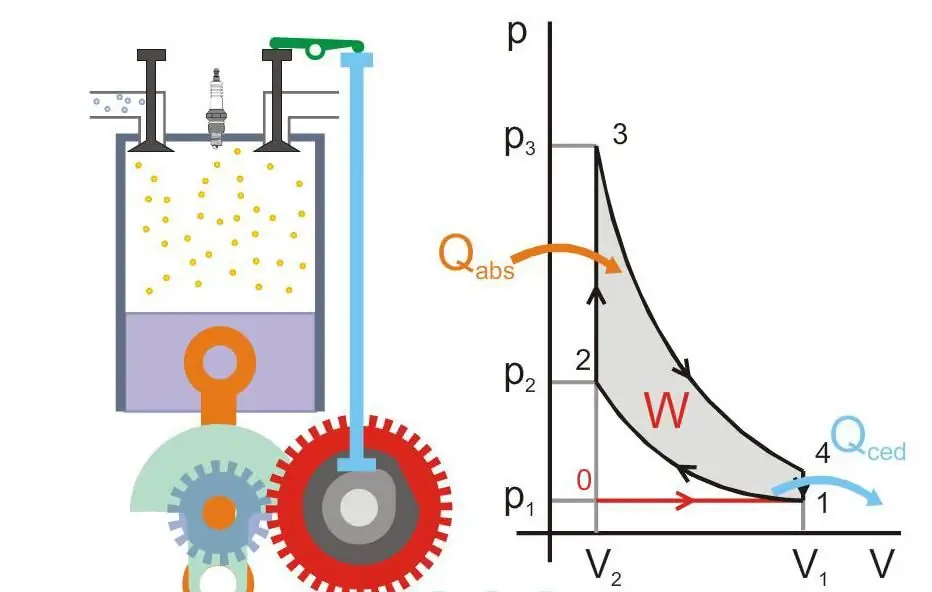
Kielelezo kilicho hapa chini kinaonyesha kanuni ya uendeshaji wa injini ya joto (Qabs - joto lililohamishwa hadi kwenye mashine, Qced - kupoteza joto, W - kazi muhimu, P na V - shinikizo na kiasi cha gesi kwenye pistoni).
Sufuri kabisa na kaulimbiu ya Nernst
Mwishowe, wacha tuendelee kwenye kuzingatia sheria ya tatu ya thermodynamics. Pia inaitwa Nernst postulate (jina la mwanafizikia wa Ujerumani ambaye aliiunda kwa mara ya kwanza mwanzoni mwa karne ya 20). Sheria inasema: "Sufuri kabisa haiwezi kufikiwa na idadi ndogo ya michakato." Hiyo ni, haiwezekani kwa njia yoyote "kufungia" kabisa molekuli na atomi za dutu. Sababu ya hii ni ubadilishanaji wa joto uliopo mara kwa mara na mazingira.

Hitimisho moja muhimu linalotolewa kutoka kwa sheria ya tatu ya thermodynamics ni kwamba entropy hupungua mtu anaposonga kuelekea sufuri kabisa. Hii ina maana kwamba mfumo huwa unajipanga. Ukweli huu unawezatumia, kwa mfano, kuhamisha sumaku-umeme hadi kwenye hali ya ferromagnetic wakati zimepozwa.
Inafurahisha kutambua kwamba halijoto ya chini kabisa ambayo imefikiwa hadi sasa ni 5·10−10 K (2003, MIT laboratory, USA).






